| Page Index |
|
|
���{�T�C�g�Ɍf�ڂ�����E�f�[�^�͎��Ö�̊J��������m�邱�Ƃ���ȖړI�Ƃ��Čf�ڂ��Ă���A�ʂ̊��҂���Ƃ��̎��ÂɊւ��ē���̎��Ö@�Ȃǂ𐄏�������̂ł͂���܂���B���ÂɊւ��Ă̔��f�́A�厡��Ȃǂ̈�Î҂Ƃ����k�̂����������łȂ����Ă��������B
�@ |
| �i���E������ᇁj |
|
|
|
����Ɋւ��铝�v |
|
| ���S�� |
����32 ��5,941 �l�i�S�����ɑ�30.1%�j�@�F�l�����Ԓ����i2005�N�j
���{�l�̂R�l�ɂP�l������Ŏ��S |
| �늳�� |
53 ���l�i�j��30.5 ���l�A����22.5 ���l�j
�j���ő������ʁF�݁A�咰�A�x�A�̑��A�O���B
�����ő������ʁF�咰�A���[�A�݁A�q�{�A�x |
| ���U���X�N |
�j��46.3%�A����34.8%
�g���{�l�j���̂Q�l�ɂP�l�A�����̂R�l�ɂP�l������ɂȂ�h |
| ��ÁE���� |
�p���I�Ȉ�Â��Ă���҂�128 ���l |
| ������ |
2 ��3,306 ���~�i�S�̂�9.6%�j |
|
|
�@����Ɋւ��铝�v�@2006�N �����J���Ȏ��� |
|
�@ |
|
�R������ᇖ�̗Տ��]�����@�Ɋւ���K�C�h���C�� |
|
(����17 �N11 ��01 �� ��H�R������1101001 ��)��蔲��
��T������
�@��T�������͔�Տ��������т���Ɏ���������߂ăq�g�ɓ��^����i�K�ł���B��Տ������Ŋώ@���ꂽ���ۂɊ�Â��A�p�ʂɈˑ�����������̈��S������������̂���ȖړI�ŁA������̓��^�o�H�A���^�X�P�W���[���A�ő�ϗʁiMTD�j���͍ő勖�e�ʁiMAD�j�A�p�ʐ����Ő��iDLT�j�A���ԂƓŐ��̊֘A���A��U�������ɂ����鐄���p�ʂ����߂�B�i��ʓI�Ȗ�܂̑�T�������́A���퐬�l�j�q�{�����e�B�A��ΏۂƂ��čs�����A�j�Ő��������R������ᇖ�̑�T�������ł́A���N�Ȑl�ł͂Ȃ��A���҂�ΏۂƂ��ׂ��ł���B�܂��A��ʓI�ɔF�߂�ꂽ�W���I���Ö@�ɂ���ĉ�����Ǐ�ɘa��������\���̂��邪�҂�ΏۂƂ��ׂ��ł͂Ȃ��B
��U������
�@��U�������́A����̊���ɑ���L�����A���S����]�����邽�߂Ɏ��{����鎎���ŁA�ΏۂƂ������ɂ����鎡����̗Տ��I�Ӌ`�̂��鎡�Ì���(�ʏ�A��ᇏk������)�A�y�ш��S����]������B
��V������
�@��V�������́A���D�ꂽ�W���I���Ö@���m�����邽�߂ɍs����Տ������ł���B��U�������ɂ����Ĉ��S���Ǝ�ᇏk�����ʁA���͉��炩�̃����b�g�i�Ǐ�ɘa���ʓ��j���m�F���ꂽ�V�K�R������ᇖ�̒P�Ɩ��͕��p�Ö@�ƓK�ȑΏƌQ�Ƃ̔�r�����ł���B���Ґ�����������i�זE�x���A�݊��A�咰���A�������j��ΏۂƂ����R������ᇖ�ł́A���ꂼ��̊���ɂ��ĉ������ʂ𒆐S�ɕ]�������V�������̐��т����F�\�����ɒ�o���邱�Ƃ�K�{�Ƃ���B |
|
�@ |
|
|
|
�@ |
|
�x���� |
|
�@�x����́A����̒��ł��ł��\��̕s�ǂȂ��̂̈�Ƃ���Ă���A���{�ł́A2005�N�̔N�ԐV�K�x����늳���Ґ��Ƃ��Ė�85,000 �l�����v����Ă��܂��B |
|
| ��ʖ� |
�u�����h�� |
����� |
�̔���� |
�������� |
���l |
| EGFR�`���V���L�i�[�[�j�Q |
�@ |
�@ |
�@ |
�@ |
�@ |
| �@�Q�t�B�`�j�u |
�C���b�T |
�זE�x���� |
�A�X�g���[�l�J |
143���~
�i2009/12�j |
2002�N ���E�ɐ�삯�ē��{�ŏ��F
2010�N ���E���� 393�S��$ |
| �@���_�G�����`�j�u |
�^���Z�o |
�i�s���זE�x����
�B������ |
���V��/���O���� |
83���~
�i2011/12�j |
2007/10/22 �������F
2012�N ���E���� 1,314�S��CHF
OSI Pharmaceuticals�ЋN�� |
| �REGFR���m�N���[�i���R�� |
�@ |
�@ |
�@ |
�@ |
�@ |
| �@�Z�b�L�V�}�u |
�A�[�r�^�b�N�X |
�זE�x���� |
�u���X�g���E�}�C���[�Y �X�N�C�u |
- |
�@ |
| �@�n�j�c���}�u |
�x�N�e�B�r�b�N�X |
�זE�x���� |
�A���W�F���A���c |
- |
�@ |
| pan-HER�`�����V���L�i�[�[�j�Q�@ |
�@ |
�@ |
�@ |
�@ |
�s�t�IErbB�t�@�~���[�j�Q��
�@�A�t�@�`�j�u |
�@ |
�x���� |
�x�[�����K�[�C���Q���n�C�� |
- |
2012/06/04 �Տ������̐��� |
| �@�_�R�~�`�j�u |
PF-00299804 |
�x���� |
�t�@�C�U�[ |
- |
2014/01/29 P3���ʂ\ |
| �@neratiniv |
PF-0528767 |
�x���� |
�t�@�C�U�[ |
- |
�@ |
| pan-HER/VEGFR2�`�����V���L�i�[�[�j�Q�@ |
�@ |
�@ |
�@ |
�@ |
| �@ |
BMS-690514 |
�זE�x���� |
�u���X�g���E�}�C���[�Y �X�N�C�u |
- |
�@ |
| HER��ʑ̉��j�Q���m�N���[�i���R���@ |
�@ |
�@ |
�@ |
�@ |
| �@pertuzumab |
�@ |
�זE�x���� |
�W�F�l���e�b�N |
�@ |
�@ |
| VEGFR�`���V���L�i�[�[�j�Q |
�@ |
�@ |
�@ |
�@ |
�@ |
| �@cediranib |
AZD2171 |
�זE�x���� |
�A�X�g���[�l�J |
�@ |
�@ |
| �@pazopanib |
���H�g���G���g�� |
�זE�x���� |
�O���N�\�E�X�~�X�N���C�� |
�@ |
�@ |
| �RVEGF��e�� �E2�R�� |
�@ |
�@ |
�@ |
�@ |
�@ |
���ǐV���j�Q��
�@Ramucirumab |
IMC-1121B |
�]�ڐ��݂���
�זE�x���� |
�C�[���C�����[�E�A���h�E�J���p�j�[ |
- |
2012/10/16 ��III�������̎�v�]�����ڂ�B�� |
Pan-VEGFR�j�Q
|
�@ |
�@ |
�@ |
�@ |
�@ |
�R������ᇍ�/�L�i�[�[�j�Q��
�@�A�L�V�`�j�u |
�C�����C�^ |
�זE�x����
�����؏��s�\���͓]�ڐ��̐t�זE���� |
�t�@�C�U�[ |
- |
2012/08/30 �������� |
| VEGFR+���� ��זE�������q (FGF)��e�� �`���V���L�i�[ �[�j�Q�j�Q�@�@�@ |
�@ |
�@ |
| �@ |
BMS582664 |
�זE�x���� |
�u���X�g���E�}�C���[�Y �X�N�C�u |
- |
�@ |
| VEGFR+EGFR +RET �`���V���L�i�[�[�j�Q�@�@ |
�@ |
�@ |
�@ |
| �@�o���f�^�j�v |
AZD6474 |
�זE�x���� |
�A�X�g���[�l�J |
�@ |
�@ |
| VEGF�A�����R���������q�iPDGF)�A FGF��e�̂̃g���v ���j�Q�@�@�@ |
�@ |
�@ |
| �@nintedanib |
�@ |
�x���� |
�x�[�����K�[�C���Q���n�C�� |
- |
�@ |
| �����������p����_���y�f�j�Q�@ |
�@ |
�@ |
�@ |
�@ |
�@ALK�j�Q��
�@�N���]�`�j�u |
�U�[�R��
(�o����)
|
�זE�x���� |
�t�@�C�U�[ |
- |
2012/10/26 ���B���F
2012/03/30 �������F
2011/05/17 ���ē����\��
ALK�j�Q�܂����E���̉����� |
| �@�`�k�j�j�Q�� |
�`�e�W�O�Q |
�זE�x���� |
���V��/���O���� |
- |
Phase2
�U�[�R���̎������ |
| MEKI�A 2�j�Q |
�@ |
�@ |
�@ |
�@ |
�@ |
| �@trametinib |
�@ |
�זE�x���� |
�O���N�\�E�X�~�X�N���C�� |
�@ |
���{�����Y�ƋN�� |
| �R�t�_��e�̃��R�� |
�@ |
�@ |
�@ |
�@ |
�@ |
| �@farletuzumab |
MORAb�E003 |
�זE�x���� |
�G�[�U�C |
- |
�@ |
| �RPDL�R�� |
�@ |
�@ |
�@ |
�@ |
�@ |
| �@���S�q�g�^�RPD-1�R�� |
ONO-4538/
BMS-936558 |
�זE�x����A
�]�ڐ��������F��A
�t�זE���� |
BMS
�����i�H�� |
- |
2012/06/04 ��T���Տ������̐��� |
| �̍זE���B���q�iHGF�j��e�̃`���V���L�i�[�[�j�Q |
�@ |
�@ |
�@ |
�@ |
�@ |
c-Met��e�̃`���V���L�i�[�[�I��I�j�Q��
�@tivantinib |
ARQ 197
�i�o���\�Ȓᕪ�q�j |
�זE�x���� |
���O��/
ArQule |
- |
2012/10/02 ��3���Տ������̒��~ |
c-Met��e�̃`���V���L�i�[�[�I��I�j�Q��
�@tivantinib |
ARQ 197
�i�o���\�Ȓᕪ�q�j |
�זE�x���� |
���a���y�L����/
ArQule |
- |
2012/08/30 ���ғo�^�ꎞ���f�i���p�����ŊԎ����x�����̔��ǁj |
| ���̑��̍�p�@�� |
�@ |
�@ |
�@ |
�@ |
�@ |
�V�R�R���������̍����ގ�������
�@�G���u�������V���_�� |
�n�����F�� |
�זE�x���� |
�G�[�U�C |
- |
�@ |
| �J���{�v���`�� |
�p���v���`���ق� |
�זE�x���� |
�u���X�g���E�}�C���[�Y �X�N�C�u�ق� |
- |
�@ |
| �p�N���^�L�Z�� |
�^�L�\�[�� |
�זE�x���� |
�u���X�g���E�}�C���[�Y �X�N�C�u |
- |
�@ |
���q�W�I���Ö�E�R�̈��
�@�x�o�V�Y�}�u |
�A�o�X�`��
Avastin
|
�i�s�E�Ĕ��̔זE�x����
�i�s�E�Ĕ��̌����E��������
�t�זE���� |
�W�F�l���e�b�N/���V��/���O���� |
564���~
�i2011/12�j |
2009/11/09 �������F
2012�N ���E���� 5,764�S��CHF |
��ӝh�R���R������ᇍ�
�@�y���g���L�Z�h�i�g���E�����a�� |
�A�����^
Alimta
|
�������������
�זE�x���� |
�C�[���C�����[ |
307���~
�i2011/12�j |
2007/01/19 ��������
2012�N ���E���� 2,594�S��$ |
| �Q���V�^�r�� |
�W�F���U�[��
Gemzar |
�זE�x����A
��p�s�\�܂��͍Ĕ�������A�X����A�_������A�A�H��炪�� |
�C�[���C�����[ |
196���~
�i2010/12�j |
1999/03/12 �������F
�X�����Â̑��I���
2010�N ���E���� 1,149�S��$ |
�A���R��
�@�h�Z�^�L�Z�� |
�^�L�\�e�[��* |
�זE�x���� |
�T�m�t�B�E�A�x���e�B�X |
- |
�^�L�T���n�̍R����܁�3
������̉��w�Ö@�̕W���I�Ȏ��Ö�
2010�N ���E���� 2,122�S���� |
�i�A�����o���R���j
�g�|�C�\�����[�[�j�Q��
�@�m�M�e�J�����_�� |
�n�C�J���`�� |
���זE�x���� |
�O���N�\�E�X�~�X�N���C��/���{�����i�̔��j |
- |
���Ăɂ����Ă͗������A���זE�x���y�юq�{����̎��Ö�Ƃ��ď��F�B
���{�ł�2001�N��菬�זE�x���̌��\�Ő����̔�
2010�N ���E���� 144�S���� |
| �V�X�v���`�� |
�u���v���`��
�����_ |
�זE�x���� |
�u���X�g���E�}�C���[�Y
���{���� |
-
12���~
�i2012/05�j |
�@ |
| �G�g�|�V�h |
�x�v�V�h
���X�e�b�g |
�זE�x���� |
�u���X�g���E�}�C���[�Y
���{���� |
-
10���~
�i2012/05�j |
���M�Ȃ̐A���ł���|�h�t�B���������Ƃɍ��ꂽ�R�����
���{�ł́A1980�N��ɓo�� |
�e�K�t�[��(Tegafur)
�E���V��(Uracil)�z�� |
���[�G�t�e�B |
�זE�x���� |
��Q��i�H�� |
157���~
�i2011/03�j |
�@�@ |
�R������ᇐ��R������
�A���g���T�C�N�����n
�@�A�����r�V�����_�� |
�J���Z�h |
�זE�x����
���זE�x���� |
����{�Z�F����
�i���{���̔��j |
- |
2012/09/05 �����\��
2002/12 �����Ŕ̔����J�n
���Ăł͓��o��̕ăZ���W�[���Ђ��Տ����������{ |
| motesanib diphosphate |
AMG706 |
�i�s��G�����זE�x���� |
���c��i�H��
�~���j�A���E�t�@�[�}�V���[�e�B�J���Y |
- |
2012/05/21 �A�W�A�����Տ���3�������̊J�n |
|
|
���x����ɑ��镪�q�W�I���Â̓����@�Ȋw�Z�p�����@2010�N7�����@�Ȋw�Z�p���������Z���^�[
�@ |
|
������ |
|
�@���E�ی��@�ցiWHO�j�ɂ��ƁA������́A���E�e���A���ʂɊW�Ȃ��A�x����Ɏ�����2�Ԗڂɜ늳���̍�������ł��B���N100���l���V���ɓ�����Ɛf�f����A40���l�ȏ�̏������Ȃ��Ȃ��Ă���ƕ���Ă��܂��B�܂��A����������Ƃ��Đf�f����鏗����30���l�ȏ�Ɛ��肳��Ă��܂��B
�@���{�ɂ����Ă�������̐V�K�늳�Ґ��͔N�X�������Ă���A2010 �N�̔N�ԐV�K������늳���Ґ���45,000�l���Ɛ��v����Ă��܂��B |
|
| ��ʖ� |
�u�����h�� |
����� |
�̔���� |
�������� |
���l |
�RHER2�q�g�����m�N���[�i���R��
�@�g���X�c�Y�}�u
�@�itrastuzumab emtansine�j |
�n�[�Z�v�`��
Herceptin
(���q�W�I���Ö�E�R�̈��) |
HER2������
�i�s�E�Ĕ��݂��� |
�W�F�l���e�b�N/���V��/���O���� |
259���~
�i2011/12�j |
2001/06 �������F
2012�N ���E���� 5,889�S���� |
�RHER2�q�g�����m�N���[�i���R��
�@pertuzumab
�@�y���c�Y�}�u |
Perjeta
�p�[�W�F�^ |
�]�ڐ������� |
���V��/���O���� |
- |
2013/06/28 �������F
2013/03 ���B���F
2012/06 ����F
Herceptin�̍�p��⊮ |
���q�W�I���Ö�E�R�̈��
�@�x�o�V�Y�}�u |
�A�o�X�`��
Avastin |
�i�s�E�Ĕ��̔זE�x����
�i�s�E�Ĕ��̌����E��������
�t�זE����
��p�s�\���͍Ĕ����� |
���V��/���O���� |
564���~
�i2011/12�j |
2011/09/26 �����lj����F
2009/11/09 �������F
2012�N ���E���� 5,764�S��$ |
�A���R��
�@�h�Z�^�L�Z�� |
�^�L�\�e�[��* |
������
�זE�x����A�݂���A������A��������A�H������A�q�{�̂���A�O���B���� |
�T�m�t�B�E�A�x���e�B�X |
- |
�^�L�T���n�̍R����܁�3
������̉��w�Ö@�̕W���I�Ȏ��Ö�
2010�N ���E���� 2,122�S���� |
�J�y�V�^�r��
�icapecitabine�j |
�[���[�_
�iXeloda�j |
��p�s�\�܂��͍Ĕ������A
�����؏��s�\�Ȑi�s�E�Ĕ��̈݊��A
�������ɂ�����p��⏕���w�Ö@�A
�����؏��s�\�Ȑi�s�E�Ĕ��̌����E������ |
���V��/���O���� |
100���~
�i2011/12�j |
2012�N ���E���� 1,523�S��CHF |
| �A�i�X�g���]�[�� |
�A���~�f�b�N�X |
�o������� |
�A�X�g���[�l�J |
210���~
�i2008/12�j |
2010�N ���E���� 1,512�S��$ |
| �t���x�X�g�����g |
�t�F�\���f�b�N�X�ؒ�250mg |
�o������� |
�A�X�g���[�l�J |
- |
2011/09/26 �����lj����F |
EGFR�iE����B1�j��HER2��2�̃`���V���E�L�i�[�[��e�̂�j�Q����o���̒ᕪ�q������
�@���p�`�j�u�g�V���_�����a��
�@�ilapatinib�j |
�^�C�P���u
(�o����) |
ErbB2�z���̓����� |
�O���N�\�E�X�~�X�N���C�� |
- |
2008/06/23 ���B���F
2009/06/19 �������F
2010�N ���E���� 227�S���� |
| �Q���V�^�r�� |
�W�F���U�[��
Gemzar |
��p�s�\�܂��͍Ĕ�������A
�זE�x����A�X����A�_������A�A�H��炪�� |
�C�[���C�����[ |
196���~
�i2010/12�j |
2010/02/10 �������F
�X�����Â̑��I���
2010�N ���E���� 1,149�S��$ |
�p�N���^�L�Z��
�i�A���u�~�������^�j |
�A�u���L�T�� |
������ |
��Q��i�H�� |
- |
2010/09/17 �����̔�
2005�N1���@�č�FDA���F
�A�u���L�V�X�E�o�C�I�T�C�G���X�E�C���N�i��Celgene�j�N�� |
�V�R�R���������̍����ގ�������
�@�G���u�������V���_�� |
�n�����F�� |
�Ǐ��i�s���E�]�ڐ������� |
�G�[�U�C |
- |
2011/05/17 �X�C�X���F
2011/04/22 ���{���F
2011/03/22 ���B���F
2011/02/10 �V���K�|�[�����F
2010/11/16 ����F
�V�K���J�j�Y����L��������ǃ_�C�i�~�N�X�j�Q�� |
| �g���~�t�F���N�G���_�� |
�t�F�A�X�g�� |
������ |
���{���� |
16���~
�i2012/5�j |
�@ |
| �R�̖����̃g���X�c�Y�}�u �G���^���V���i��`�q�g�����j�i�ʏ́FT-DM1�j |
kadeyla |
HER2�z���]�ځE�Ĕ������� |
���O���� |
- |
2013/01/25 �����\��
�|�X�g �g���X�c�Y�}�u�Ə̂����
|
mTOR�j�Q��
�@�G�x�������X |
�A�t�B�j�g�[��
Afinitor/Votubia |
������A
�]�ڐ��t�זE���� |
�m�o���e�B�X �t�@�[�} |
- |
2012�N ���E���� 797�S��$
2012/06/29 EU�ɂ����鏳�F�����擾
2010/01/20 ����P3
�X�������ᇁA���������p��A�݂���A�������Ώۂɑ�III���̍��ۋ��������ɎQ�� |
�RHER2�R�̃`���[�u�����d���j�Q�ܕ�����
�@�g���X�c�Y�}�u �G���^���V�� |
�J�h�T�C��R�_�H�� |
HER2�z���̎�p�s�\���͍Ĕ������� |
���V��/���O���� |
- |
2014/04/17 �����̔� |
| �y�O�t�B���O���X�`�� |
KRN125 |
������ |
���a���y�L���� |
- |
2013/01/25 ������V���Տ���������
���w�Ö@�ɂ��D���������ǂ̎��Ö�ł���G-CSF������2�u�O�����i��ʖ��F�t�B���O���X�`���j�v���y�O����3�������������^��G-CSF���� |
| �L�������p�N���^�L�Z���������q�~�Z���ɓ�����V�KDDS���� |
NK105 |
�]�ځE�Ĕ������� |
���{���� |
- |
2012/07/17 ��V���Տ��������J�n |
��琬�����q��e�́iEGFR/HER1�j��HER2�Ȃǂ�ErbB�t�@�~���[��I��I���s�t�I�ɑj�Q����o����
�@afatinib
�@�A�t�@�`�j�u |
Tomtovok
�i�V�K�o�����q�W�I��j |
HER2�z���]�ڐ������� |
�x�[�����K�[�C���Q���n�C�� |
- |
2010/09/17 ��V���Տ��������J�n |
�T�C�N�����ˑ����L�i�[�[�iCDK�j 4�����6��I��I�ɑj�Q
�@palbociclib |
PD-0332991
�i�o����j |
������ |
�t�@�C�U�[ |
- |
2013/04/10 FDA������I���Ö�Ɏw�� |
|
|
�咰���Ö� |
|
�@���{�ł͉ߋ�50�N�Ԃɑ咰����(CRC)�̔����������ɑ������Ă���A���݂ł͔N�Ԝ늳����95,651�l�ł��BCRC�͏����ōł���������ł���A�j���ł͈݂���Ɏ�����2�ԖڂɂȂ��Ă��܂��BCRC�͓��{�ɂ����邪��̂Ȃ���3�Ԗڂɑ������S�����ł���A����ɂ�鎀�S��7�l��1�l�ɑ������܂��B���̐����ɂ͏��f�Ő؏��s�\�ȓ]�ڐ�CRC�Ɛf�f����銳�Ґ��i��25���j���܂܂�܂��B |
|
| ��ʖ� |
�u�����h�� |
����� |
�̔���� |
�������� |
���l |
���q�W�I���Ö�E�R�̈��
�@�x�o�V�Y�}�u |
�A�o�X�`��
Avastin |
�i�s�E�Ĕ��̔זE�x����
�i�s�E�Ĕ��̌����E��������
�t�זE���� |
�W�F�l���e�b�N/���V��/���O���� |
564���~
�i2011/12�j |
2007/04/18 �������F
2012�N ���E���� 5,764�S��$ |
| �I�L�T���v���`�� |
�G���L�T�`��/�G���v���b�g |
�����E���� |
�T�m�t�B�E�A�x���e�B�X/���N���g |
292���~
�i2011/3�j |
2005/04/05 ��������
2010�N ���E���� 427�S��$
�����L������2020�N1���܂ʼn��� |
| �J�y�V�^�r�� |
�[���[�_
�iXeloda�j |
�������ɂ�����p��⏕���w�Ö@�A
�����؏��s�\�Ȑi�s�E�Ĕ��̌����E�������A
��p�s�\�܂��͍Ĕ������A
�����؏��s�\�Ȑi�s�E�Ĕ��̈݊��A |
���V��/���O���� |
100���~
�i2011/12�j |
2012�N ���E���� 1,523�S��CHF�@ |
���q�W�I���Ö�E�R�̈��
�@�A�[�r�^�b�N�X |
�Z�c�L�V�}�u |
�]�ڐ������E������ |
�u���X�g���E�}�C���[�Y �X�N�C�u�i�āA���j/
�����N�Z���[�m�i�āA���ȊO�j |
- |
2008/07/16 �������F
2010/07/02 �ŐV�Łu�咰�����ÃK�C�h���C���v�ňꎟ���Ö�ɐ���
�C���N���[���E�V�X�e���Y�ЋN�� |
���q�W�I���Ö�E�R�̈��
�REGFR���S�q�g�R��
�@�p�j�c���}�u |
�x�N�e�B�r�b�N�X�_�H�Ò� |
�i�s�E�Ĕ��̌����E�������� |
�A���W�F��
���c��i�H�� |
172���~
�i2012/3�j |
2010/04/16 �������F |
| �t�b���s���~�W���n�R���� |
�e�B�[�G�X����
(�o����) |
�����E��������A
�݂���A������A�זE�x����A��p�s�\���͍Ĕ�������A�X����A�_������ |
��Q��i�H�� |
371���~
�i2011/3�j |
���{�ł�1999�N��蔭���@ |
| ���_�C���m�e�J�� |
�J���v�g/�g�|�e�V�� |
�����E���� |
���N���g/���O�� |
29���~
�i2011/3�j |
���זE�x���A�זE�x���A�q�{�z���A�������A�L���זE���A���������p��i��z�W�L�������p��j�A�݊��A�咰���A����
2009�N�V����������
2010�N ���E���� 48���~ |
�A�t���x���Z�v�g
aflibercept |
ZALTRAP
VEGF Trap |
�����E�������� |
�T�m�t�B�E�A�x���e�B�X
Regeneron Pharmaceuticals, Inc. |
- |
2013/02/05 EU���F
2012/04/05 ���F�\������їՏ������̍ŐV���
2011/06/06 ��III��VELOUR�����̐��� |
���S���t�F�j�u
regorafenib |
�X�`�o�[�K��
Stivarga |
�����E�������� |
�o�C�G�� �w���X�P�A
Onyx  |
- |
2013/09/05 ���B�\��
2012/09/27 ����F |
| �V�K��ӝh�R���R������ᇍ܁i�z���j |
TAS-102
(�o����) |
�����E�������� |
��Q��i�H�� |
- |
2012/05/31 �O���[�o���Տ���III�������J�n |
c-Met��e�̃`���V���L�i�[�[�I��I�j�Q��
�@tivantinib |
ARQ 197
�i�o���\�Ȓᕪ�q�j |
�咰���� |
���O��/
ArQule |
- |
2013/01/15 ��2���Տ������̂̌��ʁi�ڕW�l�B�������j
2008/12 ArQule�ƒ����i���`�܂ށj�A�؍��A��p�������S���E��ARQ 197�̋����J���E���Ɖ��̃��C�Z���X�_������ |
|
|
�݂��Ö� |
|
|
|
| ��ʖ� |
�u�����h�� |
����� |
�̔���� |
�������� |
���l |
�RHER2�q�g�����m�N���[�i���R��
�@�g���X�c�Y�}�u |
�n�[�Z�v�`��
(���q�W�I���Ö�E�R�̈��) |
�i�s�E�Ĕ��݂���
HER2������ |
���V��/���O���� |
259���~
�i2011/12�j |
2010/01 ���B�ŏ��F
2011/03/10 �������F
2012�N ���E���� 5,889�S���� |
| �J�y�V�^�r�� |
�[���[�_
�iXeloda�j |
�����؏��s�\�Ȑi�s�E�Ĕ��̈݊��A
��p�s�\�܂��͍Ĕ������A
�������ɂ�����p��⏕���w�Ö@�A
�����؏��s�\�Ȑi�s�E�Ĕ��̌����E������ |
���V��/���O���� |
100���~
�i2011/12�j |
2010/08/30 ���m�\��
2012�N ���E���� 1,523�S��CHF |
| �t�b���s���~�W���n�R���� |
�e�B�[�G�X����
(�o����) |
�݂���A
������A�����E��������A�זE�x����A��p�s�\���͍Ĕ�������A�X����A�_������ |
��Q��i�H�� |
371���~
�i2011/3�j |
2011/03/15 �i�s���݂���̈ꎟ���Ö�Ƃ��ĉ��B�ŏ��F
���{�ł�1999�N��蔭�� |
�A���R��
�@�h�Z�^�L�Z�� |
�^�L�\�e�[��* |
������
�זE�x����A�݂���A������A��������A�H������A�q�{�̂���A�O���B���� |
�T�m�t�B�E�A�x���e�B�X |
- |
�^�L�T���n�̍R����܁�3
������̉��w�Ö@�̕W���I�Ȏ��Ö�
2010�N ���E���� 2,122�S���� |
| �V�X�v���`�� |
�u���v���`��
�����_ |
�Ίێ�ᇁA�N�����A�t᱁E�A�ǎ�ᇁA�O���B���A�������A�����A�זE�x���A�H�����A�q�{����A�_�o��זE��A�݊��A���זE�x���A������A��זE��ᇁi������ᇁA������ᇁA���B�O��ᇁj |
�u���X�g���E�}�C���[�Y�j
���{���� |
19���~
�i2010/05�j |
�@ |
�RVEGFR�]2�q�gIgG1�^���m�N���i�[���R�́F���ǐV���j�Q��
�@Ramucirumab
�@�����V���}�u |
IMC-1121B |
�]�ڐ��݂��� |
�C�[���C�����[�E�A���h�E�J���p�j�[ |
- |
2012/10/16 ��III�������̎�v�]�����ڂ�B�� |
mTOR�j�Q��
�@�G�x�������X |
�A�t�B�j�g�[��
Afinitor/Votubia |
�݂���A
�]�ڐ��t�זE���� |
�m�o���e�B�X �t�@�[�} |
- |
2012�N ���E���� 797�S��$2010/01/20 ����P3
�X�������ᇁA���������p��A�݂���A�������Ώۂɑ�III���̍��ۋ��������ɎQ�� |
c-Met��e�̃`���V���L�i�[�[�I��I�j�Q��
�@tivantinib�F�`�o���`�j�u |
ARQ 197 |
�݂��� |
���a���y�L����/
ArQule |
- |
P2�J�n�i���{�Ȃ�тɃA�W�A�̈ꕔ�i�����A�؍�����ё�p�j |
|
|
�O���B���� |
|
�@�O���B����͐��E��3�Ԗڂɑ�������ł���A�j���̂���ɂ�鎀�S���̑�6�ʂ��߂Ă��܂��B���ۂ����@�ւɂ��ƁA���B�ł�2004�N��23��8,000�l�̒j�����O���B����Ɛf�f����A8��5,000�l���O���B����ɂ���Ď��S���܂����B
�č��ł́A2007�N�ɂ͖�21��9,000�l�̒j�����O���B����Ɛf�f����A2��7,000�l�ȏオ���̎����ɂ���Ď��S����Ɨ\������Ă��܂��B���B�A���iEU�j�ł́A���N20���l�ȏ�̒j�����V���ɑO���B����Ɛf�f����A6���l�ȏオ�O���B����ɂ���Ď��S����Ɨ\������Ă��܂��B
�O���B����̔������͔N��ƂƂ��ɏ㏸���邽�߁A�Љ�̍�����i�ނɂ�O���B����̊��҂̐�������ɑ������邱�Ƃ��\�z����܂��B
�@���{�l�j���̑O���B����늳���i2005�N�j��3��7,060�l�Ɛ��v����Ă���A�j���ł͈݂���A�咰����A�x����A�̑�����Ɏ�����5�Ԗڂɑ����A���S����6�Ԗڂɍ�������ł��2
����Ґl���̑����ɔ����A���{�ɂ�����O���B����̜늳���͂��ꂩ�����������Ɨ\�z����Ă��܂��B |
|
| ��ʖ� |
�u�����h�� |
����� |
�̔���� |
�������� |
���l |
| �|�_�����[�v�������� |
�����[�v���� |
�O���B���E�o�O�����E�q�{�����ǁE�q�{�؎� |
���c��i�H�� |
678���~
�i2012/3�j |
2012/3 ���E���� 1,207���~ |
�A���R��
�@�h�Z�^�L�Z�� |
�^�L�\�e�[��* |
�O���B����A
������A�זE�x����A�݂���A������A��������A�H������A�q�{�̂��� |
�T�m�t�B�E�A�x���e�B�X |
- |
2008/09/01 �������F
�^�L�T���n�̍R�����
2010�N ���E���� 2,122�S���� |
| �S�Z�������|�_�� |
�]���f�b�N�X
Zoladex |
�O���B����
�o�O������ |
�A�X�g���[�l�J |
- |
2012�N ���E���� 1,093�S��$ |
�R�A���h���Q����
�@�r�J���^�~�h |
�J�\�f�b�N�X |
�O���B���� |
�A�X�g���[�l�J |
453���~
�i2008/12�j |
2010�N ���E���� 579�S��$ |
| �@ |
�G�X�g���T�C�g |
�O���B���� |
���{�V�� |
26���~
�i2010/3�j |
�@ |
| �t���^�~�h |
�I�_�C�� |
�O���B���� |
���{���� |
31���~
�i2012/5�j |
�@ |
�|�_�A�r���e����
�iAbiraterone Acetate�j |
ZYTIGA |
�]�ڐ��̋�����R���O���B���� |
Johnson & Johnson |
������ |
2012/06/04 ��������
2011/04/28 ����F |
| �f�K�����N�X�|�_�� |
�S�i�b�N�X�牺���p |
GnRH�A���^�S�j�X�g/
�O���B���� |
�A�X�e���X���� |
- |
2012/10/22 �����̔� |
���̍R�A���h���Q����
�@p-INN |
�G���U���^�~�h
XTANDI
(�o����) |
�O���B���� |
Medivation/
�A�X�e���X���� |
- |
2013/06/24 ���B���F�擾
2012/09/14 �����
2009/10/28 ��Medivation�Ђ�蓱�� |
| ��X�e���C�h�n�̒j���z�����������y�f�j�Q�� |
TAK-700 |
�i�s���O���B���� |
���c��i�H�� |
- |
2013/07/26 �Տ���3�������̒��ԉ�͂Ɋ�Â� �ӌ�����
2012/06/05 �Տ������̍ŐV�f�[�^
2012/01/27 ���{�@P3�J�n
2010/11/04 ��@P3�J�n |
| Alpharadin |
�@ |
�O���B���� |
Bayer |
- |
2011/06/06 �č�P3�ŗǍD�Ȍ��� |
| ����y�v�`�h���N�`���uITK-1�v |
�e�[���[���C�h�^����y�v�`�h���N�`���uITK-1�v |
�O���B���� |
�x�m�t�C���� |
- |
2013/07/03 ������III ���Տ������J�n |
|
|
�̂���A�̍זE���Ö� |
|
�@�̂���͐��E��6�Ԗڂɜ늳���̍�������ŁA���N�V����60���l�ȏオ�̂���Ɛf�f����܂��B�킪���ł̊̂���̜늳�Ґ��͖��N�V���ɖ�4���l�ł���A��3��5��l�̕������S���Ă���A����ɂ�鎀���̑�3�ʂł��B
�@�������̂���́A�̍זE����ƒ_�ǍזE����ɑ�ʂł��A������94�����̍זE����ł��B�̍זE����̑�����B�^�����C�^�̉��E�C���X�ւ̊����������ł���A���{�ł�C�^�̉��E�C���X�ւ̊������̂���̔��nj����̖�67�����߂Ă��܂��B
�@�̍זE����́A�����p��̍Ĕ�������r�I�������Ƃ��m���Ă���A����C�^�̉��E�C���X�z���̍זE���Ì�1�N�ڂ܂ł�24%�A3 �N�ڂ܂ł�76%�A5�N�ڂ܂ł�92%�ƕ���Ă��܂��B |
|
| ��ʖ� |
�u�����h�� |
����� |
�̔���� |
�������� |
���l |
���q�W�I����
�@�\���t�F�j�u |
�l�N�T�o�[��
(�o����) |
�̍זE����A
�����؏��s�\�܂��͓]�ڐ��̐t�זE���� |
�o�C�G����i |
- |
�o�C�G���ƃI�j�L�X�E�t�@�[�}�V���[�e�B�J���Ђŋ����J�� |
| �~���v���`�����a�� |
�~���v�� |
�̍זE���� |
����{�Z�F���� |
13���~
�i2012/3�j |
2009/10/16�@�������F |
c-Met��e�̃`���V���L�i�[�[�I��I�j�Q��
�@tivantinib�F�`�o���`�j�u |
ARQ 197 |
�̍זE���� |
���O��
ArQule |
- |
2013/02/01�@��3���Տ������J�n�i���{�A����(���`���܂�)�A�؍��A��p�������S���E�j
2012/06/04�@��2���Տ��������� |
| �y���`�m�C�� |
NIK-333 |
�̍זE����Ĕ��}���� |
���a |
- |
2010/05/24 �����\�������� |
c-Met��e�̃`���V���L�i�[�[�I��I�j�Q��
�@tivantinib�F�`�o���`�j�u |
ARQ 197 |
�̍זE���� |
���a���y�L����/
ArQule |
- |
P1�J�n�i���{�Ȃ�тɃA�W�A�̈ꕔ�i�����A�؍�����ё�p�j |
|
|
�t�זE���Ö� |
|
�@�t���ɔ������鈫����ᇂ̂ЂƂŔA�Ǐ��זE�����������̂ł��B�D���N���50�Έȍ~�Œj����͖�2�F1�ł��B���{�ɂ�����t�זE���̊��Ґ���10,000�l�ȏ�ƌ����Ă��܂��B�ߔN�ACT�╠�������g�����Ȃǂ̉摜�f�f�Z�p�̐i���ƌ��f�̕��y�Ȃǂɂ�葁���ɔ��������ǗႪ�����Ă��܂��B��p�ɂ��a���̐؏������Â̊�{�ł����A�����؏��s�\�܂��͓]�ڐ��̐i�s��̏ꍇ�́A����܂ŗL���Ȏ��Ö@�͂���܂���ł����B |
|
| ��ʖ� |
�u�����h�� |
����� |
�̔���� |
�������� |
���l |
���q�W�I����
�@�\���t�F�j�u |
�l�N�T�o�[��
(�o����) |
�̍זE����A
�����؏��s�\�܂��͓]�ڐ��̐t�זE���� |
�o�C�G����i |
- |
2008/01 �������F
�o�C�G���ƃI�j�L�X�E�t�@�[�}�V���[�e�B�J���Ђŋ����J�� |
���q�W�I���Ö�E�R�̈��
�@�x�o�V�Y�}�u |
�A�o�X�`��
Avastin |
�i�s�E�Ĕ��̔זE�x����
�i�s�E�Ĕ��̌����E��������
�t�זE���� |
�W�F�l���e�b�N/���V��/���O���� |
564���~
�i2011/12�j |
2012�N ���E���� 5,764�S��$ |
mTOR�j�Q��
�@�G�x�������X |
�A�t�B�j�g�[��
Afinitor/Votubia |
�����؏��s�\���͓]�ڐ��̐t�זE���� |
�m�o���e�B�X �t�@�[�} |
- |
2012�N ���E���� 797�S��$
2010/04/16 �����̔�
2011�N12�����X�_�o�������ᇂ̎��Ö�Ƃ��ď��F
���ߐ��d���ǂɑ��Ă͌��ݐ\����
|
�L�i�[�[�j�Q��
�@�X�j�`�j�u�����S�_�� |
�X�[�e���g
Sutent |
�����؏��s�\���͓]�ڐ��̐t�זE��
�C�}�`�j�u��R���̏����NJԎ���� |
�t�@�C�U�[ |
- |
2008/04/18 �������F
2012�N ���E���� 1,236�S��$ |
mTOR�j�Q��
�@�e���V�������X |
�g�[���Z�� |
�����؏��s�\���͓]�ڐ��̐t�זE�� |
�t�@�C�U�[ |
- |
2010/09/17 �������� |
�R������ᇍ�/�L�i�[�[�j�Q��
�@�A�L�V�`�j�u |
�C�����C�^ |
�����؏��s�\���͓]�ڐ��̐t�זE�� |
�t�@�C�U�[ |
- |
2012/08/30 �������� |
ANYARA
�@interferon-alpha���p�� |
�@ |
�t�זE���� |
Active Biotech AB |
- |
2013/01/29 Phase II/III ���ʔ��\ |
| �R�̈�� |
AGS-16M8F |
�]�ڐ��t�זE���� |
�A�W�F���V�X(�č�)�F�A�X�e���X����n�� |
- |
2010/09/01 �č�P1�J�n |
�g���v�����Ǔ���זE���B���q�iVEGF�j��e�̑j�Q��
�@�`�{�U�j�u�iTivozanib�j |
ASP4130
(�o����) |
�i�s���t�זE���� |
�A�X�e���X����
AVEO Oncology |
- |
2012/09/28 ��\��
2012/05/17 ��III���Տ������iTIVO-1�j�̗ǍD�Ȏ������� |
|
|
�������� |
|
�@��������͎��o�ǏR�������ƂȂǂ���A��������������ł���A�\��s�ǂ̎�ᇂ̈�ł���Ƃ����Ă��܂��B�܂��A���̜늳���Ґ��͔N�X�����X���ɂ���A���l�Ɏ��S�Ґ����������Ă��܂��B�����āA�늳���҂̔N����̂����Ɣ�r���ĒႭ�A�s�[�N�늳�N���50�`54�Ƃ����Ă��邽�߁A�Ĕ��̉\������r�I�����Ĕ������ۂɎg�p�ł����܂����Ȃ����Ƃ���A�C�O�ɂ�����Ĕ���������̕W�����Ö�̏��F���҂��]�܂�Ă��܂��B |
|
| ��ʖ� |
�u�����h�� |
����� |
�̔���� |
�������� |
���l |
| �h�L�\���r�V�����_�� |
�h�L�V�� |
���w�Ö@��ɑ��������������� |
�����Z���t�@�[�} |
- |
2009/04/23 �������F
1999�N�̕č�����ɐ��E��80�J���ŏ��F |
�A���R��
�@�h�Z�^�L�Z�� |
�^�L�\�e�[��* |
��������
�݂���
�q�{�̂���
�H������
������
�זE�x����
������ |
�T�m�t�B�E�A�x���e�B�X |
- |
�^�L�T���n�̍R����܁�3
������̉��w�Ö@�̕W���I�Ȏ��Ö�
2010�N ���E���� 2,122�S���� |
| �Q���V�^�r�����_�� |
�W�F���U�[��
Gemzar |
���w�Ö@��ɑ������������� |
�C�[���C�����[ |
196���~
�i2010/12�j |
2010/08/30 ���m�\�� |
| �m�M�e�J�����_�� |
�n�C�J���`�� |
���w�Ö@��ɑ������������� |
���{����/�O���N�\�E�X�~�X�N���C�� |
- |
2010/08/30 ���m�\��
2010/09/03 �����\��
2010�N ���E���� 144�S���� |
���q�W�I���Ö�E�R�̈��
�@�x�o�V�Y�}�u |
�A�o�X�`��
Avastin |
�i�s�E�Ĕ��̔זE�x����
�i�s�E�Ĕ��̌����E��������
�t�זE���� |
�W�F�l���e�b�N/���V��/���O���� |
564���~
�i2011/12�j |
2011/06/09 �Ĕ���������̕a���i�s�̃��X�N��
2012�N ���E���� 5,764�S��$ |
���m�N���[�i���R��
�@farletuzumab
�@�t�@�����c�Y�}�u |
MORAb-003 |
�������� |
�G�[�U�C |
- |
2013/01/11 ��III���Տ������̑���
2012�N�x���Đ\���\�� |
|
|
�X������ |
|
�@����������͐i�s�������A�܂���������ɂ�������ł��B���̂��߁A�������ꂽ���ɂ͂��łɂ����Ȃ�i�s���Ă���A��p���s���Ȃ��P�[�X�����Ȃ�����܂���B��ʓI�ɂ��������X�e�[�W�Wa�A�Wb�ł͎�p������A�R������Â���ː����Â��s���܂��B |
|
| ��ʖ� |
�u�����h�� |
����� |
�̔���� |
�������� |
���l |
| �Q���V�^�r�� |
�W�F���U�[��
Gemzar |
�X������i�X����j
�_������
�זE�x����
�Ĕ��E�i�s������ |
�C�[���C�����[ |
196���~
�i2010/12�j |
�X�����Â̑��I��� |
| �p�N���^�L�Z�� |
�A�u���L�T�� |
�]�ڐ��X������ |
Celgene |
- |
2013/09/06 FDA���F |
| �����́iADC�j |
ASG-5ME |
�]�ڐ��B������ |
Seattle Genetics
�A�X�e���X���� |
- |
2013/01/25 P1�����̐��т\ |
���q�W�I���Ö�E�ᕪ�q��
�@�G�����`�j�u |
�^���Z�o |
�i�s���זE�x����
�B������ |
���V��/���O���� |
83���~
�i2011/12�j |
2009/09/18 �X����ɑ�����\�E���ʒlj��̏��F�\��
2012�N ���E���� 1,314�S��CHF
OSI Pharmaceuticals�ЋN�� |
| �t�b���s���~�W���n�R���� |
�e�B�[�G�X����
(�o����) |
�݂���A
������A�����E��������A�זE�x����A��p�s�\���͍Ĕ�������A�X����A�_������ |
��Q��i�H�� |
- |
2011/06/08 �Տ�����(GEST) ���ʂ�č��Տ���ᇊw��(ASCO)�Ŕ��\ |
|
|
������������iMM�j���� |
|
�@������������́A���t����̒��łQ�Ԗڂɑ��������ł��B���ۍ�������c�i�h�l�e�j�ɂ��ƁA�S���E�ł̑�����������̑����Ґ��́A��V�T�O�C�O�O�O�l�Ɛ�������Ă��܂��B�����J���Ȃ̓��v�ɂ��Ɠ��{�ł̑�����������̑����Ґ��͖�P�P�C�O�O�O�l�ŁA���N��S�C�O�O�O�l���V���ɐf�f����Ă��܂��B |
|
| ��ʖ� |
�u�����h�� |
����� |
�̔���� |
�������� |
���l |
| �{���e�]�~�u |
�x���P�C�h |
������������ |
�~���j�A��/
�����Z���t�@�[�}
�i���c��i�H���j
|
- |
2012/03 ���E���� 581���~
2006/10/20 �������F
�v���e�A�\�[���Ƃ����y�f�̓�����}�����p�����V�����^�C�v�̍R����܁B
��Millennium���n��
2009�N�̑S���E�̔��㍂��10���ăh���B |
| ���i���h�~�h���a�� |
���u���~�h |
�Ĕ����͓���̑�����������Ö� |
Celgene Corporation |
- |
2010/06/25 �������F�B
�f�L�T���^�]���Ƃ̕��p�Ö@�Ƃ��Đ��E�T�O�J���ȏ�ŏ��F |
| pomalidomide |
POMALYST |
�Ĕ����͓���̑�����������Ö� |
Celgene Corporation |
- |
2013/02/08 ����F |
| �V�K�v���e�A�\�[���j�Q�� |
MLN-9708
(�o����) |
�Ĕ��E��������������� |
�~���j�A��/
�i���c��i�H���j |
- |
2012/06/29 P3���ۋ��������J�n
2012/06/04 �Տ������̍ŐV�f�[�^�ɂ���
2011/06/13�@��1�������f�[�^�ɂ���
|
| �@ |
Kyprolis |
�Ĕ���������������� |
Onyx Pharmaceuticals
�����i |
- |
2012/06/21 ODAC���J�C�v�����X�̎g�p�𐄏�
�����ł̓t�F�[�Y�T/�U���������{�� |
|
|
�����������a�iCML�j���� |
|
�@���������������a�iCML�j�́A�̓��Ŗ����ُ̈�Ȕ����������������A�������i�s����^�C�v�̔����a�ł��B�ŐV�̓��v�ł́A�č��Ŗ�22,475�l�����̕a�C�ɜ늳���Ă��܂��B2009�N�ɂ́A5,050�l���V����CML�Ɛf�f���ꂽ�Ɛ��肳��܂��B CML�́A2�̈قȂ���F�̂��ؒf����A�݂��Ɍ������邱�Ƃɂ���Ĕ��ǂ��܂��B���̐V���ɐ��������F�̂̓t�B���f���t�B�A�z�����F�̂ƌĂ�A�ߏ�Ȕ������זE������悤�זE�ɃV�O�i���𑗂�BCR-ABL�Ƃ����ُ�Ȉ�`�q���܂�ł��܂��BCML�������N������`�q�ω��̌����͖��炩�ɂ͂Ȃ��Ă��܂���B |
|
| ��ʖ� |
�u�����h�� |
����� |
�̔���� |
�������� |
���l |
���q�W�I���Ö�E�ᕪ�q��
�`���V���L�i�[�[�j�Q��
�@���V���_�C�}�`�j�u |
�O���x�b�N
Gleevec/Glivec |
�����������a |
�m�o���e�B�X �t�@�[�} |
- |
2012�N ���E���� 4,675�S��$ |
���q�W�I����
�@�j���`�j�u���_�����a�� |
�^�V�O�i
Tasigna |
���������������a |
�m�o���e�B�X �t�@�[�} |
- |
2012�N ���E���� 998�S��$
�č��A���B�Ȃǐ��E50�����ȏ�Ŕ���
2010/12/21 ���������������a�̈ꎟ���Ö�Ƃ��č������F
2009/01/21 �������F
2010/08/28 ���������������a�̈ꎟ���Ö�Ƃ��ăX�C�X�ŏ��F |
| �_�T�`�j�u���a�� |
�X�v���Z�� |
�����������a |
�u���X�g���E�}�C���[�Y �X�N�C�u/��ː��� |
- |
2011/06/16 ���������������a�̃t�@�[�X�g���C�����Ö�Ƃ��ď��F
�����̔����F���F2009/1/21
2010/12/07�F�C�}�`�j�u�Ƃ̔�r�����̒ǐՌ���
2010/06/08�F�C�}�`�j�u�Ƃ̔�r��������
2010�N ���E���� 576�S��$ |
| �O�_���q�f���ˉt |
�g���Z�m�b�N�X |
�Ĕ����͓���̋}���O�������������a���Í� |
���{�V�� |
- |
2004/12 �����̔�
�Z�t�@�����ЋN�� |
DNA���`�����j�Q��
�@decitabine |
Dacogen
�i���ˍ܁j |
�}�������������a |
�G�[�U�C |
- |
�������ٌ`���nj�Q�iMDS�j�̓K���ŕč��ŏ��F���擾 |
| NEDD8�������y�f�j�Q��Ƃ��ď��߂ėՏ��i�K�ɐi�t�@�[�X�g�C���N���X�̖�� |
MLN-4924 |
�}�������������a����уn�C���X�N�̍����ٌ`���nj�Q |
�~���j�A��/
�i���c��i�H���j |
- |
2011/06/13�@��1�������f�[�^�ɂ���
|
|
|
���l�s�זE�����a�iATL�j���Ö� |
|
�@���l�s�זE�����a�i�`�s�k�j�́A�u�g�s�k�u�|�P�v�Ƃ����E�C���X�������N�������t�̂���B�����̊����Ґ��͂P�O�O���`�Q�O�O���l�Ƃ݂����B�������甭�ǂ܂ł̐������Ԃ������i��T�O�`�U�O�N�̐��������j�̂������ŁA�T�����x�����ǂ��A���N��P�P�O�O�l�����S����B���̃^�C�v�̔����a�Ɣ�ׂč����ڐA��R����܂������ɂ����A���{�I�Ȏ��Ö@�͊m������Ă��Ȃ����A�U���ȏ�͕����ʂ��Ċ������邱�Ƃ���A���{�͔D�w���f�łg�s�k�u�|�P�����ׂ�R�̌�����p������ŕ��S���Ă���B�`�s�k�͔����a�̒��ł��ł����Â�����B����̍R����܂�g�ݍ��킹�����Âł́A���ǂ����l�̖����P�N�ȓ��Ɏ��S����Ƃ���Ă���B�ق��̊����ǂŎ��S���邱�Ƃ������B�R����܂��g�����w�Ö@�Ȃǂ������ɂ����A���Â�����Ƃ���Ă���B����זE�͑̊O����N�������ٕ��ł͂Ȃ����߁A�Ɖu�זE�̍U�����ɂ����B�������A�u�m�x�\�d�r�n�\�P�v�Ƃ�������ς���������A�Ɖu�זE���ٕ��Ƃ��čU�����邱�Ƃ��������Ă���B
|
|
| ��ʖ� |
�u�����h�� |
����� |
�̔���� |
�������� |
���l |
�q�g�����m�N���[�i���R��
�@���K�����Y�}�u |
�|�e���W�I�_�H�� |
���l�s�זE�����a |
���a���y�L���� |
- |
2012/03/30 �������F
�Ĕ����͓����CCR4�z���̐��lT�זE�����a�����p��iATL�j��1�̎��Ö� |
|
|
�������F��i�����m�[�}�j���� |
|
�@�������F��i�����m�[�}�j�́A�畆�ɂ���F�f�זE�i�����m�T�C�g�j�̖������ȑ��B������Ƃ���畆����̈�`�Ԃł��B�]�ڐ��������F��́A���̕a�C�̒��ł��ł��v�����������A�畆�\�ʂ����łȂ��A���̑���i�����p�߁A�x�A�]�A���̑��̕����j�ɂ����]�ڂ��ċN����܂��B�ꕔ�̂���זE�́A�Ɖu�n�̊Ď���ϋɓI�ɓ���邱�Ƃ�����A���̂��߂Ɏ�ᇂ��c��܂��B�����m�[�}�́A�����Ɏ��Â���A�啔���������\�ł��B�������Ȃ���A�����ł́A���ϐ������Ԃ͂킸��6�J���ԁA1�N���S����75%�ł���A�ł��N�P���̍����a�Ԃ����������1�ƂȂ��Ă��܂��B�č��ł͔N�ԂW�V�O�O�l�����S���Ă��܂��B |
|
| ��ʖ� |
�u�����h�� |
����� |
�̔���� |
�������� |
���l |
���S�q�g�RCTLA-4�R�̐���
�@ipilimumab�i�C�s�����}�u�j |
Yervoy |
�؏��s�\�܂��͓]�ڐ��������F�� |
Bristol-Myers Squibb |
- |
2011/03/25 FDA���F |
�ᕪ�q���i
�@vemurafenib |
Zelboraf
�iPLX4032�j
(�o����) |
�]�ڐ��������F�� |
�o����������������
�i���O���j |
- |
2012/02/20 ���B���F
2011/08/18 FDA���F
Plexxikon�ЋN��
���V���O���[�v�Ƌ����J�� |
BRAF�j�Q��
�@dabrafenib
MEK�j�Q��
�@trametinib |
TAFINLAR
MEKINIST |
BRAF V600��`�q�ψٗz���̐؏��s�\�܂��͓]�ڐ������m�[�} |
�O���N�\�E�X�~�X�N���C�� |
- |
2013/05/29 ����F
2012/08/06 ���Đ\��
MEK�j�Q�܂����{�����Y���N�� |
BRAF/MEK���p�j�Q��
�@dabrafenib
�@trametinib |
�@ |
BRAF�z�������m�[�} |
�O���N�\�E�X�~�X�N���C�� |
- |
2013/02/01 P3�J�n |
| ATP�h�R�IBRAF�L�i�[�[�j�Q�� |
GSK2118436 |
BRAF�̕ψق�L���鍕�F��̔]�]�� |
�O���N�\�E�X�~�X�N���C�� |
- |
�@ |
| NEDD8�������y�f�j�Q�� |
MLN4924 |
�]�ڐ����F�� |
Millennium Pharmaceuticals, Inc.
�i���c��i�j |
- |
2011/06/07 �Տ���1�������f�[�^�ɂ��� |
|
|
���������p��� |
|
���������p��́A�������̒��̃����p������������������ŁA�S�g�̃����p�߂���ꂽ��A��ᎂ��ł����肷��a�C�ł��B���̈��������p��ɂ́A�傫�������āu�z�W�L�������p��v�Ɓu��z�W�L�������p��v������܂��B�z�W�L�������p��́A��{�I�Ƀ��[�h�[�V���e�����x���O�זE��z�W�L���זE�ȂǁA�����I�ȑ�^�זE���F�߂��邱�ƂŐf�f����܂��B���������p��́A�킪���ł́A�N��10���l������V�`�W�l�ɔ������܂����A�z�W�L�������p��͖�10���Ə��Ȃ��A�唼����z�W�L�������p��ł��B���{�ɂ������z�W�L�������p��̔��ǐ��͔N�Ԗ�12,000�l�Ɛ��肳��A�ߔN�����X���ł���Ƃ���Ă��܂��B |
|
| ��ʖ� |
�u�����h�� |
����� |
�̔���� |
�������� |
���l |
���q�W�I���Ö�E�R�̈��
�@���c�L�V�}�u |
���c�L�T��/�}�u�Z��
MabThera/ Rituxan |
��z�W�L�������p�� |
���ުݥ���ޯ�
/���V��/���O���� |
229���~
�i2011/12�j |
�q�gB�זE�\�ʍR���̈�ł���CD20��W�I�Ƃ��郂�m�N���[�i���R�́B
2012�N ���E���� 5,622�S��$ |
| �x���_���X�`�����_�� |
Symbenda |
�Ĕ��܂��͓���̒ራ���x��z�W�L�������p��
�}���g���זE�����p�� |
�V���o�C�I
�G�[�U�C |
- |
2010/12/10 �����̔�
�����ƃC�G�i�t�@���}�ЋN�� |
�V�K�̃q�g���m�N���[�i���R��
�@�I�t�@�c���}�u
�@Ofatumumab |
Arzerra |
������������p�������a |
�O���N�\�E�X�~�X�N���C�� |
- |
2010/04/26 ���B���F |
Brentuximab Vedotin
�u�����^�L�V�}�u �x�h�`�� |
�A�h�Z�g���X |
�Ĕ��E����̃z�W�L�������p�� |
Seattle Genetics, Inc./
Millennium Pharmaceuticals, Inc.
�i���c��i�j |
- |
2014/04/17 �����̔�
2013/02/01 �J�i�_���F
2012/10/31 ���B���F |
�������ό^�^�C�v�U�RCD20���m�N���[�i���R��
�@Obinutuzumab |
GA101 |
�ራ���x����ђ��������x��z�W�L�������p�� |
Genentech, Inc.
���O����
���{�V�� |
- |
2013/01/31 P3�����ɂĖ��������p�������a���҂̐������ԉ�����B�� |
| �y�O�t�B���O���X�`�� |
KRN125 |
���������p�� |
���a���y�L���� |
- |
2013/01/25 ������V���Տ���������
���w�Ö@�ɂ��D���������ǂ̎��Ö�ł���G-CSF������2�u�O�����i��ʖ��F�t�B���O���X�`���j�v���y�O����3�������������^��G-CSF���� |
|
|
���̑��̂��Ö� |
|
| ��ʖ� |
�u�����h�� |
����� |
�̔���� |
�������� |
���l |
�A���R��
�@�h�Z�^�L�Z�� |
�^�L�\�e�[�� |
������
�q�{�̂���
�H������ |
�T�m�t�B�E�A�x���e�B�X |
- |
�^�L�T���n�̍R����܁�3
������̉��w�Ö@�̕W���I�Ȏ��Ö�
2010�N ���E���� 2,122�S���� |
�A�����o���R��
�@�m�M�e�J�����_�� |
�n�C�J���`�� |
�q�{�� |
�O���N�\�E�X�~�X�N���C��
���{���� |
- |
���Ăɂ����Ă͗������A���זE�x���y�юq�{����̎��Ö�Ƃ��ď��F�B
���{�ł�2001�N��菬�זE�x���̌��\�Ő����̔�
2010�N ���E���� 144�S���� |
| �~�t�@�����`�h |
���p�N�g |
��]�ڐ������� |
���c��i�H�� |
������ |
2010/02/01 ���B�Ŕ̔� |
| �{���m�X�^�b�g |
MK-0683 |
�畆T�זE�������p�� |
MSD
�i��Q��i�H�Ɓj |
- |
2011/06/14 ��Q��i�H�ƂƓ��{�����ɂ�����̔��_������
2010/06/30 �����\�� |
| �q�g�����m�N���[�i���R�� |
KW-0761 |
���w�Ö@�t����̍Ĕ����͍ĔR���lT�זE�����a�����p��iATL�j |
���a���y�L���� |
- |
2011/04/26 �����\��
�R�̈��Ƃ��Ă͏��̂`�s�k���Ö� |
|
|
���A���R��
�@�A���̐������璊�o�������́B
��2 ���q�W�I����
�@����זE�݂̂�W�I�ɂ��č��ꂽ���i�B
��3 �^�L�T���n�̍R�����
�@�C�`�C�̎��琬�����猩�������V�R�������B�זE�̕���ɕK�v�ȁ������ǁi�`���[�u�����j�����ǂ����艻���邱�ƂōזE�����j�Q���A�ŏI�I�ɂ���זE�̎��łɂȂ���ƍl�����Ă��܂��B
��4 �A���X���T�C�N�����n�̍R�����
�@�A���g���T�C�N�����n��DNA�\���ڔj�܂��B���w�Ö@�ōł��זE��Q�����������̂̂ЂƂł���ƍl���Ă��܂��B
��5 ���l�s�זE�����a�i�`�s�k�j
�@��ɕ������Ċ�������E�C���X�g�s�k�u�P�������̓�����t����B���������҂͂P�O�O���l�ȏ�ŋ�B�E����ݏZ�҂������߂�B���ǂ���ƌ��t���Ŕ����a�זE�����B���A�Ɖu�@�\���ቺ������A�����p�߂Ɏ�ᇂ��ł����肷��B�������Ԃ����ςT�T�N�ƒ����A�����҂̐��U���Ǘ��͖�T���ƒႢ���A�L���Ȏ��Ö@�͖��m���B���N���l���S���Ȃ��Ă���B
�@ |
|
�@ |
|
�V���Ȏ��Ö@�@�Ɖu�Ö@�i���N�`���Ö@�j |
|
�@����זE�ɂ͂Ȃ��A����זE�����ɂ��邪��R�������N�`���Ƃ��đ̓��ɒ������A�����F�������l�̂��R�̂�����Ă���R�����U������Ƃ����A�l�̖̂Ɖu�����𗘗p�����d�g�݂ł��B
�@�����ł͂悤�₭�Տ��������͂��܂�������̎��Ö@�ł��B���������ȃ����p���ړ��Ö@�����זE�Ö@�ȂǂƑg�ݍ��킹�邱�ƂŁA�����ʓI�Ȏ��Â��ł���̂ł͂ƍl�����Ă��܂��B |
|
| �u�����h�� |
�̔���� |
�������� |
���l |
�q�{��\�h���N�`��
�u�T�[�o���b�N�XR�v |
�O���N�\�E�X�~�X�N���C�� |
517���~
�i2011/12�j |
2009/10/16�@�������F
2007�N5���ɃI�[�X�g�����A�ŏ��߂Ă̏��F���擾
2010�N ���E���� 242�S����
�q�{��̖�70���̌������߂�Ƃ����q�g�p�s���[�}�E�C���X�iHPV�j��16�A18�^�ɑ��ėL�� |
�q�{��\�h���N�`��
GARDASIL�i�K�[�_�V���j |
Merck & Co., Inc.
MSD |
- |
2011/07/01�@�������F
2006�N6���ɁA���E�ŏ��߂ĕč��ŏ��F
2012�N ���E���� 1,631�S��$
16�A18�^�̂ق��A��\�R���W���[�}�̖�90���̌����ł���6�A11�^�ɂ��L�� |
| MAGE-A3�F�זE�x����A�������F�� |
�O���N�\�E�X�~�X�N���C�� |
- |
��V���Տ�����
MAGE-A3��W�I�R���Ƃ�������ς������N�`�� |
����y�v�`�h�J�N�e�����N�`���Ö@��
OCV-C01�F�X������ |
�I���R�Z���s�[�E�T�C�G���X |
- |
2012/08/13 ��V���Տ������J�n |
| �咰���×p�y�v�`�h�J�N�e�����N�`�� |
��ː���
�I���R�Z���s�[�E�T�C�G���X |
�@ |
2013/01/07 ��T���Տ������J�n |
���×p�y�v�`�h���N�`��
ONO-7268MX1�F�̍זE���� |
�����i�H��
�I���R�Z���s�[�E�T�C�G���X |
�@ |
2012/07/02 ��T���Տ������J�n |
| L-BLP25�F�זE�x���� |
�����i�H��
�����N�Z���[�m |
�@ |
2012/12/19 �s�{�^����V�������ɂ����Ď�v�]�����ڂ�B������ |
�N�������×p���N�`��
S-288310�F�N���� |
����`����
�I���R�Z���s�[�E�T�C�G���X |
�@ |
2009/11/04 ��T�^�U���Տ������J�n |
���×p���N�`��
S-488410�F�H������ |
����`����
�I���R�Z���s�[�E�T�C�G���X |
�@ |
2010/09/14 ��T�^�U���Տ������J�n |
�y�v�`�h���N�`��
S-646240�F������ϐ� |
����`����
�I���R�Z���s�[�E�T�C�G���X |
�@ |
�t�F�[�Y�Ua�������{�Ӓ� |
�V�����Ǒj�Q��
OTS102�F�_������ |
�}�K��i�H��
��ː���
�I���R�Z���s�[�E�T�C�G���X |
�@ |
2012/02/29 �������Ԃ̗D�ʍ��F�߂�ꂸ
2008/12/16 �X���ɑ�����U/�V���Տ����� |
��ᇍR����W�I�Ƃ��邪�N�`���Ö@��
OCV-105
|
��ː���
�I���R�Z���s�[�E�T�C�G���X |
�@ |
2011/06/13 �X�����ɑ����T���Տ������J�n |
WT1�W�I���N�`��
OCV-501�F�}�������������a
|
��ː��� |
�@ |
������T���Տ��������{��
���Ɖu�������Ƌ����J�� |
��ᇐV�����Ǔ���זE��W�I�Ƃ��邪�N�`���Ö@��
OCV-101�F�X������
|
��ː���
�I���R�Z���s�[�E�T�C�G���X |
�@ |
2011/06/07 �č��Տ���ᇊw��iASCO�j2011 ���\
2011/02/01 �؏��s�\�i�s�X��������эĔ��X������ΏۂƂ�����U���Տ������J�n |
�������×p���N�`��
CHP-NY-ESO-1�F�H������ |
�C�~���m�t�����e�B�A |
�@ |
2009/12/01 ��T���Տ������J�n |
ZYC300�@CYP1B1���R���Ƃ���Ɖu�Ö@���N�`��
E6020�@����TLR4�쓮�� |
�G�[�U�C |
�@ |
��T���Տ�������
�O�Տ� |
���×p����y�v�`�h���N�`���uWT4869�v
�����ٌ`���nj�Q�iMDS�j��Ώ� |
����{�Z�F���� |
�@ |
2013/04/08 ���O����Ƃ̋����J���I��
2010/12/21 ������T�^�U���Տ����� |
| �e�[���[���C�h�^����y�v�`�h���N�`���uITK-1�v |
�x�m�t�C���� |
- |
2013/07/03 ������III ���Տ������J�n |
| DCVax-Brain�F�]��� |
Northwest Biotherapeutics |
- |
���҂̎���זE�Ƃ���זE�̐�����p�������N�`��
2007 �X�C�X���F |
| Provenge�F�O���B���� |
Dendreon Corporation |
- |
����R������ς�����Y���������җR���̎���זE���N�`��
2010 ����F |
| ���J�j�b�N�X�F�זE�x���� |
NovaRx Corporation |
- |
���B�}����`�q���������Ǝ�ᇍזE
��V���Տ����� |
| PROSTVAC�F�O���B���� |
Bavarian Nordic A/S |
- |
�V�R���E�C���X���x�N�^�[�ɗp�����זE���N�`��
��V���Տ����� |
| IMA901�F�i�s���t�זE���� |
immatics biotechnologies GmbH |
- |
�����̐t�����N�`���֘A�̃y�v�`�h��p�������N�`��
��V���Տ����� |
| ������ |
CEL-SCI Corporation |
- |
2013/02/01 Northeast Ohio Medical University�ƃR���{���[�V�����\ |
|
|
�@ |
|
|
|
�@ |
|
|
|
|
|
�@ |
| �i��ӌn�����j |
|
|
|
�@���ۓ��A�a�A���̏W�v�ɂ��Ɠ��A�a�̊��Ґ��́A�S���E��3���l�ɔ����Ă���A2030�N�ɂ�4��3500���l�ɑ�����Ɨ\������Ă��܂��B�������Ґ��͐����740���l�A�^�킵���l���܂߂��1620���l�ɂ̂ڂ�A����30�N�Ԃ�30�{�ɖc��݂܂����B
�@���A�a�ɂ͎�N�҂ɋ}���ɔ��ǂ���1�^�ƁA�H����^���Ȃǂ̐����K�����W����Ƃ����2�^�Ȃǂ�����A2�^�͓��{�l�̓��A�a��9���ȏ���߂Ă��܂��B�@���A�a�ŋ��낵���̂́A���������ǁB�����̐悪���т�A�₪�đg�D�̉��s�i�����j�ɂ��Ȃ���u�_�o��Q�v�A���o����Ԗ��͂����Ȃǂ��N���������Ɏ���u�Ԗ��ǁv�A�t���̂�ߋ@�\���ቺ���ŏI�I�ɂ͐l�H���͂��K�v�ɂȂ�u�t�ǁv���O�升���ǂł��B
�@���A�a�́A��`�a��ꕔ�̂���̂悤�ɓ���̈�`�q�ُ̈�ɂ���Ĕ��ǂ���̂ł͂Ȃ��A10�`15�N�̐����K���ƈ�`�q�v�����d�Ȃ菉�߂ċN���܂��B�@�C���X�����́A�X���ɂ��郉���Q���n���X�����E�a�זE���番�傳��A���t���̃u�h�E�����זE���ɑ���G�l���M�[�ɕς�����A�]���ȃu�h�E���������肵�āA�����l��������z�������ł��B�B���A�a�Ƃ́A�C���X�����̕���ɏ�Q���N�����āA�G�l���M�[���ƂȂ铜���̗��p���\���ɍs�����A�����i���t���̓����j���オ�肷���Ă��܂��a�C�ł��B
�@���A�a���Ö�͑傫�������Č����l�߂���C���X�����z�������̓��^�ƁA����Ō����l�����������܂��B�C���X�������^�͎�ɁA�C���X�����傷���X���i���������j�̃��זE�����ȖƉu�����Ȃǂɂ��ꂽ�P�^���A�a���Ҍ����B�����~����p����̂́A�ߐH��^���s���A����Ȃǂ��d�Ȃ蔭�ǂ���Q�^���A�a���҂ł��B�S�̖̂�95�����߂܂��B
�@ |
|
�@ |
|
�C���X�������呣�i�� |
|
�X���t�H�j���A�f�n��܁iSU�j
�@�X���̃��זE���h�����邱�Ƃɂ��C���X��������𑣐i���铜�A�a���Ö�ł��B |
|
| ��ʖ� |
�u�����h�� |
�̔���� |
�������� |
���l |
| ��Q�����@�O���y���N���~�h |
�I�C�O���R�� |
���O���� |
- |
�@ |
�X���z�j���E���A�n�����~����
�@�O���N���W�h |
�O���~�N����
(�o����) |
����{�Z�F���� |
28���~
�i2011/03�j |
�@ |
�X���z�j���E���A�n�����~����i��R����j
�@�O�����s���h |
�A�}���[��
(�o����) |
�T�m�t�B |
- |
2013/01/15 OD��0.5mg �V����
2010�N ���E���� 478�S���� |
|
|
�@ |
|
�����^�C���X�������呣�i�� |
|
�@�]���̃C���X�������呣�i��i�r�t��j�ɔ�ׁA���p�㑬�₩�Ɍ��ʂ����邱�Ƃ���A�C���X������������R�ȃp�^�[���ɋ߂Â��ĐH�㍂���������P���܂��B��p�������Ԃ��Z�����߁A�]���̂r�t��ɔ�גጌ������N���ɂ����A�܂��X���̃��זE�̔敾���y�����邱�Ƃ����҂���Ă��܂��B
�@�C���X�������܂̒������^�́A���ˌ�10�`20���Ō��ʂ��\��܂��B�ȑO�̑����^�͒��ˌ�A��p����܂łɖ�30��������A�H�O�̒��˂ƐH���̎��Ԃɂ��ꂪ������ƁA�H��̍�������Ԃ����܂����P�ł��Ȃ����Ƃ�A�t�Ɍ����l�𐳏펞���������Ă��܂��ꍇ������܂����B
�@�C���X������21�̃A�~�m�_����Ȃ�`���ƁA30�̃A�~�m�_����Ȃ�a�������������|���y�v�`�h�B�������^�̓A�~�m�_�z��̈ꕔ��ς��ċz������₷�������B2001�N����f���}�[�N�̃m�{�m���f�B�X�N���u�m�{���s�b�h�v���A�ăC�[���C�����[���u�q���[�}���O�v����{�Ŕ̔����Ă��܂��B |
|
| ��ʖ� |
�u�����h�� |
�̔���� |
�������� |
���l |
�������^�C���X�����A�i���O����
�@�C���X���� �A�X�p���g�FIAsp |
�m�{���s�b�h |
�m�{ �m���f�B�X�N |
- |
�@ |
�������^�C���X�����A�i���O����
�@�C���X���� ���X�v���i��`�q�g�����j |
�q���[�}���O |
�C�[���C�����[ |
- |
�@ |
�����^�C���X�������呣�i��
�@�~�`�O���j�h�J���V�E�����a�� |
�O���t�@�X�g |
�L�b�Z�C��i�H��
���c��i�H�� |
51���~
49���~
�i2011/3�j�@ |
�@ |
�����^�C���X�������呣�i��
�@�i�e�O���j�h�@ |
�t�@�X�e�B�b�N |
���̑f�|���O�� |
52���~
�i2010/3�j |
�@ |
| �X�^�[�V�X |
���̑f�|�A�X�e���X���� |
49���~
�i2005�N�j |
2012/10/10 DPP-4�j�Q�܂Ƃ̕��p�����Ɋւ��鋤���J���_�������@ |
�����^�C���X�������呣�i��
�@���p�O���j�h |
�V���A�|�X�g |
����{�Z�F���� |
- |
2011/05/09 ��������
�č��ł́uPrandin�v�A���B�ł́uNovoNorm�v�̐��i���Ŕ̔��BNovo Nordisk��蓱�� |
|
|
�@ |
|
�����^�C���X�������� |
|
�@�牺����̋z���������₩�ł��邽�߁A�]���̒��Ԍ^�C���X�������܂ɔ�ׂČ����C���X�����Z�x�̃p�^�[���Ƀs�[�N������܂���B�܂��A�قڈ���ɂ킽���č�p���������A��Ԃ̒ጌ�������Ȃ��Ƃ�������������܂��B |
|
| ��ʖ� |
�u�����h�� |
�̔���� |
�������� |
���l |
�����^�n���C���X��������
�@�C���X�����E�O�����M���i��`�q�g�݊����j |
�����^�X
Lantus
�i�牺�����j |
�T�m�t�B�E�A�x���e�B�X |
- |
2012�N ���E���� 4,960�S���� |
�����^�C���X���� �A�i���O���ˉt
�@�C���X���� �f�O���f�N�i��`�q�g�����j |
�g���V�[�o |
�m�{ �m���f�B�X�N |
- |
2012/09/28 �������� |
|
|
�@ |
|
�H��ߌ������P�� |
|
��-�O���R�V�_�[�[�j�Q�܁i��-GI�j
�@�����S���ɑ��݂��郿�O���R�V�_�[�[�Ƃ����y�f�́A������Y���������u�h�E���ɕ������铭�������Ă��܂��B���̖�́A���̃��O���R�V�_�[�[�̓���������܂��邱�ƂŁA�u�h�E���ւ̕�����x�点�܂��B���̌��ʂƂ��āA�u�h�E���̑̓��ւ̋z�����������ɂȂ�A�H��ߌ������}�����܂��B���{�ōł��g�p����Ă���2�^���A�a���Í܂̈�ł��B |
|
| ��ʖ� |
�u�����h�� |
�̔���� |
�������� |
���l |
���A�a�H��ߌ������P��
�@�A�J���{�[�X |
�O���R�o�C |
�o�C�G����i |
140���~
�i2005�N�j |
�@ |
���A�a�H��ߌ������P��
�@�{�O���{�[�X |
�x�C�X�� |
���c��i�H�� |
259���~
�i2012/3�j |
�@ |
���A�a�H��ߌ������P��
�@�~�O���g�[�� |
�Z�C�u�� |
����{�Z�F���� |
- |
�@ |
|
|
�@ |
|
�C���X������R�����P�� |
|
�r�O�A�i�C�h�n��܁iBG�j
�@�̑��ɂ����铜�V���}����p�A�����ǂɂ����铜�z���}����p�A�����g�D�ɂ�����C���X���������P��p������Č������������܂ŁA�����ł́A���g�z���~�����_���i���i���u���g�O���R���v���j�A�u�z���~�����_���i���i���u�W�x�g�X���v���j���̔�����Ă��܂��B |
|
<
| ��ʖ� |
�u�����h�� |
�̔���� |
�������� |
���l |
| ���g�z���~�����_�� |
�����r�� |
����{�Z�F���� |
44���~
�i2011/3�j |
1961�N�@���{�ŏ��F |
| ���g�z���~�����_�� |
�O���R���� |
���{�V�� |
9���~
�i2007�N�j |
�@ |
| ���g�z���~�����_�� |
���g�O���R
(�o����) |
����{�Z�F���� |
3���~
�i2011/3�j |
2010/04/22�@���{�Ŕ���
Merck Sante �Ђ�蓱�� |
| �u�z���~�����_�� |
�W�x�g�X�� |
����H�ق� |
- |
�@ |
|
|
�@ |
|
�`�A�]���W���n��܁iTZD�j
�@�A�o���f�B�A�iGSK�j�ƃA�N�g�X�i���c�j�̓C���X������R�����P��ƌĂ�A���b�זE�̃C���X�����ւ̊����x�����߂܂��B���S���̊m�ۂ�������đ��͑������ŊJ���Ɏ��s���A���݂͂Q�܂����̔�����Ă��܂���B
�@1999�N�ɔ����������c�́u�A�N�g�X�v�̕]���������B����グ�͐��E��2000���~���A���Ђ̎��v�̒��Ɉ���Ă��܂����B�J�����ɂ͕s����������p�@���̉𖾂��i�݁A�A�N�g�X���j����e�́i�o�o�`�q���j�Ƌ����������邱�Ƃ��������Ă��܂����B�o�o�`�q���́A���b�זE�̕����𑣂����A����ɂ��C���X�����̗����������Ȃ�����^�̎��b�זE���A�C���X�����������₷�����^�̎��b�זE�ɕω�����Ƃ���Ă��܂��B�܂����b�זE�͗l�X�Ȑ������������i�A�f�B�|�J�C���j���o���A���̒��ɂ̓C���X�����ւ̒�R�������߂�u���ʁv�ƁA�C���X�����̊������߂�u�P�ʁv������܂��B�o�o�`�q���́A�P�ʂ̎Y���𑝂₵�ăC���X�����𗘂��₷�������p������悤�ł��B |
|
| ��ʖ� |
�u�����h�� |
�̔���� |
�������� |
���l |
| ���_�s�I�O���^�]�� |
�A�N�g�X* |
���c��i�H�� |
318���~
�i2012/3�j |
1999�N �̔��J�n
2011/3 ���E���� 2,962���~ |
| �}�C�����_���V�O���^�]�� |
�A�o���f�B�A |
�O���N�\�E�X�~�X�N���C�� |
- |
2010�N ���E���� 440�S���� |
| �@ |
S-707106 |
����`���� |
- |
2010�N3�� FTIH�F�q�g�ւ̍ŏ��̓��^�����ifirst time in human study)�i�č��j
|
|
|
�@ |
|
DPP4�j�Q�� |
|
�c�o�o�S�j�Q�܁i�W�y�v�`�W���y�v�`�_�[�[-4�j�Q��j
�@�H��ɕ��傳���C���N���`���i�����̓��Z�x�Ɉˑ����ăC���X��������𑣐i��������ǃz�������̑��́j���A�I��I�ɕ�������y�f�W�y�v�`�W���y�v�`�_�[�[�i�c�o�o�j-�S��j�Q���邱�Ƃɂ��A�����^�C���N���`���Z�x���㏸�����A�����ˑ��I�Ɍ����~����p��������܂ŁA�����ł̓V�^�O���v�`�������_�����a���i���i���u�W���k�r�AR���v�A�u�O���N�e�B�uR���v�j�A�A���O���v�`���������_���i���i���u�l�V�[�iR���v�j�����̔�����Ă��܂��B
�@�E�����㓜�A�a���Í܁@DPP4�j�Q�܁ASGLT�j�Q�܊J�������@
�@ |
|
|
|
�@ |
|
GLP-1��e�̃A�S�j�X�g |
|
�@���ݍ����ŏ��F����Ă��铜�A�a���Ö�Ƃ͑S���قȂ��p�@���Ō����~����p�������V�����N���X�̖�܂ł��BGLP-1�̓q�g�̑̓��Ɏ��R�ɑ��݂��鏬�����番�傳�������ǃz�������ŁA�����l�ɉ����ăC���X��������𑣐i���܂��B
���u�A�S�j�X�g�v�Ƃ́A���̓��̎�e�̂ɓ����āA�_�o�`�B������ �z������ �ȂǂƓ��l�̍�p������쓮��B |
|
| ��ʖ� |
�u�����h�� |
�̔���� |
�������� |
���l |
| �����O���`�h |
�r�N�g�[�U |
�m�{ �m���f�B�X�N |
- |
�q�g��GLP-1��97%�̑�������L����B
2009/07/08 ���B�ŏ��F
2010/01/20 ���{�ŏ��F
2010/01/29 �č��ŏ��F
2010�N ���E���� 23��1,700��DKK�i��421���~�j |
| �G�L�Z�i�`�h |
�o�C�G�b�^ |
�C�[���C�����[ |
- |
2010/10/27 �������F
2005�N�ɕč��Ŕ��� |
Lixisenatide
�i���L�V�Z�i�`�h�j |
���L�X�~�A
�i1��1�^�j
��b�C���X�����Ƃ̕��p�� |
�T�m�t�B |
- |
2013/02/04 ���B�ŏ��F
2013/06/28 ���{�ɂ����鐻���̔����F
Zealand Pharma A/S�ЋN�� |
| �G�L�Z�i�`�h |
�r�f�����I���牺��
�i�T1�^�j |
�A�X�g���[�l�J
�u���X�g���E�}�C���[�Y |
- |
2013/05/16 �������F |
albiglutide
�i�A���r�O���`�h�j |
�@ |
�O���N�\�E�X�~�X�N���C�� |
- |
2013/01/14 �č��Ő\�� |
Taspoglutide
�i�^�X�|�O���`�h�j |
BIM 51077
R1583
ITM-077 |
�C�v�Z��/���V��
���O����/��l�t�@�[�} |
- |
�C�v�Z���Ђ��n������GLP-1�ɗގ������������B
2010/02/11 ���� P3 5�����ŗL�ӂȉ��P��p������
���{ P2 |
|
|
�@ |
|
SGLT�j�Q�� |
|
SGLT1�j�Q�� |
|
|
|
��SGLT1�iSodium-dependent Glucose Transporter
1�j�F
�@���̐��̓��ł̗A���ɂ�����铜�g�����X�|�[�^�[�̈�B�����ɑ������݂��Ă���A�����ǂł̓��z���̎�v�Ȗ�����S���Ă��܂��BSGLT1�j�Q�܂́ASGLT1�̓����ڑj�Q���ē��̏����Njz����}�����܂��B
�@ |
|
SGLT2�j�Q��
�@SGLT2�j�Q�܂̓����Ƃ��ẮA�A���r����p�ɂ�荂���������P����B�̏d�������ʂ⌌���~����p�Ȃǂ����҂ł���B�C���X��������Ȃ����ߒጌ���̃��X�N���Ⴍ�A�܂��A���̌o�������ቺ�܂�C���X�����ƕ��p���鎖���\�Ȃǂ�����܂��B |
|
|
|
��SGLT2�iSodium-dependent Glucose Transporter
2�j�F
�@���̐��̓��ł̗A���ɂ�����铜�g�����X�|�[�^�[�̈�B�t���ɓ��ٓI�ɑ��݂��Ă���A�t���ł̓��ċz���̎�v�Ȗ�����S���Ă��܂��B�����̓��͈�U�t���ł�߂���A���Ɉڍs���܂����ASGLT2�����t���ɓ���߂��܂��B
|
|
�@ |
|
�O���R�[�X�ˑ����C���X�������呣�i��iGPR40�쓮��j |
|
| ��ʖ� |
�u�����h�� |
�̔���� |
�������� |
���l |
| �iGPR40�쓮��j |
TAK-875 |
���c��i�H�� |
- |
2013/12/27 �J�����~
2011/10/17 �ĉ�P3�J�n
2011/09/12 ����P3�J�n
2011/06/29 �Տ������̍ŐV�f�[�^�ɂ���
2013�`15�N�ɐ����̔����F��ڎw���B
���A�a���Ö�̐V�K��p�@���i��������敾�������ɃC���X�����̕���𑣂��j�Ƃ��Ċ��� |
|
|
�@ |
|
GPR119��e�̃A�S�j�X�g |
|
�@GPR119�iG�^���p�N�������^��e��119�j�́A�����ǂ��X���ɑ��݂����e�̂ł��B�X���̃��זE�ɒ��ڍ�p���A�C���X�����̕���𑣐i�B����ɁA��������̃C���N���`��GLP-1�̕���𑣂��܂��B |
|
| ��ʖ� |
�u�����h�� |
�̔���� |
�������� |
���l |
| GPR119��e�̃A�S�j�X�g |
MBX-2982 |
Metabole/�T�m�t�B�E�A�x���e�B�X |
- |
��II���Տ��������{��
2010/07/05 �T�m�t�B��A�x���e�B�X��Metabolex�ЁA �Ɛ�I�O���[�o�����C�Z���X�_������ |
| GPR119��e�̃A�S�j�X�g |
DS-8500 |
���O�� |
- |
P1�������{�� |
|
|
�@ |
|
�z���� |
|
�@�Q��ވȏ�̐�������̐��܂ɔz��������̂ŁA�ʁX�ɕ��p������A���������߁A���ݖY������Ȃ����邱�Ƃ��ł��܂��B�z���܂͐��@�����G�ŁA�W�F�l���b�N���[�J�[�̂ǂ��ł��ȒP�ɒǐ��ł�����̂ł͂Ȃ��̂ŁA������̐攭��Ɠ�������Ă��Ȃ����А��i��g�ݍ��킹�Ĕ̔����邱�ƂŁA���А��i�̐��i���������邱�Ƃ����݂��Ă��܂��B |
|
| ��ʖ� |
���i�� |
�̔���� |
�������� |
���l |
| DPP4+SGLT2�̍��� |
empagliflozin and linagliptin |
�x�[�����K�[�C���Q���n�C���A�C�[���C�����[ |
- |
2014/04/14 ��\�� |
| SGLT2�j�Q�܁i�J�i�O���t���W���j�Ƒ��������g�z���~���j�̍��� |
VOKANAMET |
Johnson & Johnson |
- |
2014/04/24 ���B���F |
| �A�N�g�X�i�s�I�O���^�]�����_���j�ƃ��g�z���~���i�r�O�A�i�C�h�n��܁j�̍��� |
Actoplus met
Competact
���^�N�g |
���c��i�H�� |
- |
2005/08 �č��ŏ��F
2006/07 ���B�ŏ��F
2010/04/16 �������F
2�^���A�a���Í܂Ƃ��Ă͓��{�ŏ��߂ď��F���ꂽ�z���� |
| �A�N�g�X�i�s�I�O���^�]�����_���j�ƃX���z�j���E���A�n��܁iSU�܁j�̍��� |
�\�j�A�X |
���c��i�H�� |
- |
2011/06/06 �������� |
| �l�V�[�i�i�c�o�o�S�j�Q�܁j�ƃ��g�z���~�����_���̍��� |
KAZANO
���I�x�� |
���c��i�H�� |
- |
2013/09/24 ���B���F
2013/01/26 ����F
2011/09/20 �������� |
| �l�V�[�i�i�c�o�o�S�j�Q�܁j�ƃX���z�j���E���A�n��܁iSU�j�̍��� |
�@ |
���c��i�H�� |
- |
2011/02/23 �������F |
| �l�V�[�i�i�c�o�o�S�j�Q�܁j�ƃr�O�A�i�C�h�n��܁iBG�j�̍��� |
�@ |
���c��i�H�� |
- |
2011/02/23 �������F |
| �l�V�[�i�i�c�o�o�S�j�Q�܁j�ƃ`�A�]���W���n��܁iTZD�j�Ƃ̕��p���\�lj� |
�@ |
���c��i�H�� |
- |
2010/08/20 �������F |
| �l�V�[�i�i�c�o�o�S�j�Q�܁j�ƃA�N�g�X�i�s�I�O���^�]�����_���j�̍��� |
OSENI |
���c��i�H�� |
- |
2013/09/24 ���B���F
2013/01/26 ����F
2012/06/20 ���B�\�� |
| �����^�C���X�������呣�i��/�H��ߌ������P��z���� |
�O���x�X |
�L�b�Z�C��i�H�� |
- |
2011/04/22 �������F |
| �r���_�O���v�`���iGalvus�j�ƃ��g�t�H���~���̔z���� |
Eucreas |
�m�o���e�B�X �t�@�[�} |
- |
2008/03/06 ���B�ŏ��F |
| �V�^�O���v�`�� (�W���k�r�A)�ƃV���o�X�^�`��(���|�o�X�ق�)�̔z���� |
JUVISYNC |
Merck |
- |
2011/10/13 ����F |
| �V�^�O���v�`�� (�W���k�r�A)�ƃ��g�z���~���̔z���� |
JANUMET |
Merck |
- |
2012�N ���E���� 1,659��$ |
| �����^�C���X�����A�i���O �g���V�[�o�ƒ������^�C���X�����A�i���O
�m�{���s�b�h�̔z���� |
���C�]�f�O |
�m�{�m���f�B�X�N�t�@�[�} |
- |
2012/12/31 �������F |
| ���i�O���v�`��(Tradjenta)�ƃ��g�z���~���̔z���� |
Jentadueto |
�x�[�����K�[�E�C���Q���n�C����/�����[ |
- |
2012/02/01 ����F |
|
|
�@ |
|
|
|
�@�t���̖����͂��낢�날��܂����A���̒��S�I�ȋ@�\�́A�̓��ň�����悻200���b�g�����̌��t����߂��A�s�v�Ȑ�����L�Q������̊O�ɔA�Ƃ��Ĕr�o���邱�Ƃɂ���܂��B�t���a�́A���̐t���̋@�\���ቺ���A�V�p����]���ȕ����E�������O�ɔr�o�ł��Ȃ��Ȃ�a�C�i�t���j�ł��B
�@�����̖����t���a�̊��Ґ��́A���悻400���l�ɒB����� ����܂��B ���̕a�C�̎�ȏǏ�͂���ς��A�E���A�E�ނ��݁E������ �Ȃǂł����A�t���a�̎�ނɂ���Ă��A�Ǐ�͂��܂��܂ɈقȂ��Ă��܂��B |
|
�i�t���n�����Ö�j�F�����t���a�̍����ǂ̂����ł��p�x�̍������� |
|
| ��ʖ� |
�u�����h�� |
�̔���� |
�������� |
���l |
| �G�|�G�`�� |
�G�|�W�G��/�v���N���b�g/�G�X�|�[ |
�A���W�F��/J&J/���a���y�L���� |
618���~
�i2011/12�j |
���E����51���h���i2009�N�j |
| ��`�q�g�����q�g�G���X���|�G�`������ |
NeoRecormon
�G�|�W�� |
���V��/���O���� |
288���~
�i2011/12�j |
2010�N ���E���� 1,285�S��CHF |
| �����^�Ԍ��������h�����q���� |
R744 |
���O���� |
- |
2009/07/22 �����\��
�C�O�ł�Mircera�̐��i����2007 �N�ɔ��� |
| �Ԍ����Y���𑣐i����z�������ł���G���X���|�G�`���̎�e�̂ɍ�p���鍇���y�v�`�h�@ |
Hematide |
���c��i�H�� |
- |
2012/03/28 �č��̔����擾
2012/02/27 ���B�\��
2010/02/18 �Տ���3�������J�n�i�����j
2011�N�x���̏��F�\����\��
Affymax, Inc.��蓱�� |
|
|
�i�A�ŏǓőf�z���܁j |
|
| ��ʖ� |
�u�����h�� |
�̔���� |
�������� |
���l |
| - |
�N�����W��
�i�o���z���Y�j |
���O�� |
128���~
�i2009/3�j |
2009/10/05 �N���n�������������܂�c�ӎO�H���d����đ��O���ɋ���
1991�N�@�����̔�
�����ǂŕ���܂��͒��ǂŎY�������A�ŏǓőf���z�����A�ւƂƂ��ɑ̊O�ɔr�� |
| - |
MP-146 |
�c�ӎO�H���� |
- |
2006/11/08 �N�����W���̕ĉ��ł̓Ɛ�I�J���E�̔������N���n���擾
���Ăo�R���{���B2011�N�x�\���\�� |
|
|
�i���������ǎ��Ö�j�F
�@�t���̋@�\���������͒��̕��͐t���ł̃����̔r�o���ł��Ȃ�����
���t���̃����̔Z�x�������Ȃ��Ă��܂��܂��B�����Ń������z�����̊O�֏o���g���܂��B |
|
|
|
�i���̑��̎��Ö�j�F |
|
| ��ʖ� |
�u�����h�� |
�̔���� |
�������� |
���l |
| �����t�s�S�̓��͌^�l�H�t���̟t |
�L���_���[ |
�}�K��i�H�� |
131���~
�i2009/3�j |
- |
���J���E�����lj��P��
�@�|���X�`�����X���z���_�J���V�E�� |
�A�[�K���C�g |
�O�a���w������/
�A�X�e���X���� |
- |
2013/01/10 ��������
���Ǔ��̃J���E���C�I����{�܂̃J���V�E���C�I���ƌ������邱�Ƃɂ��A�ߏ�ƂȂ����J���E����̊O�ɔr�����邱�ƂŁA�}������і����t�s�S�ɔ������J���E�����ǂ����P����B |
|
|
|
|
�@�얞�ǂ́A�S���E��4���l�ȏオ�늳���A�������̎����̜늳���X�N�㏸�Ɗ֘A���閝�������ł��B�č��얞�w��ɂ��ƁA�얞�ǂ͕č��ɂ�����2�Ԗڂɉ���\�Ȏ��S�����Ƃ���Ă��܂��B�č��ł͑̏d�ߑ�����є얞�ǂ���т��̊֘A�����̎��Âɗv���鑍�R�X�g�͔N�Ԃ�1,400���h���ɒB���Ă��܂��B�얞�ǂ́A��i�����┭�W�r�㍑�ŋ}���ɑ������Ă���A�傫�ȎЉ���ƂȂ��Ă��Ă��܂��B |
|
| ��ʖ� |
�u�����h�� |
�̔���� |
�������� |
���l |
| ���قőI��I�ȃZ���g�j��2C(5-HT2C)��e�̃A�S�j�X�g�@�@�@lorcaserin hydrochloride�i�����J�Z�����j |
BELVIQ |
Arena Pharmaceuticals/
�G�[�U�C |
- |
2012/06/28 ����F
2011/05/26 3�̃t�F�[�YIII�̃��^���̗͂ǍD�Ȍ��ʂ\
2010/07/01 �A���[�i�E�t�@�[�}�V���[�e�B�J���Y�ƃG�[�U�C
�č��ɂ����郉�C�Z���X�_������ |
| Phentermine and Topiramate Extended-release�i�z���܁j |
Qsymia |
VIVUS, Inc. |
- |
2012/07/17 ����F
�H�~�}����uphentermine�v�ƍR�Ă��u�g�s���}�[�g�v�Ƃ̍��� |
| �}�W���h�[�� |
�T�m���b�N�X |
�m�o���e�B�X �t�@�[�} |
- |
�����Ŕ̔�����Ă���얞�ǖ�
�]�̐H�~�����ɒ��ڍ�p����,�H�~��ቺ������ |
���p�[�[�j�Q��
�@�I�����X�^�b�g |
�[�j�J��
�A���C |
���V��
�O���N�\�E�X�~�X�N���C�� |
������ |
�X�C�X�E���V�����J�������R�얞��
���b�����y�f�ł��郊�p�[�[��s���������A���b�z����j�Q |
���p�[�[�j�Q��
�@�Z�`���X�^�b�g |
�I�u���[�� |
���c��i�H��Norgine BV |
- |
2013/09/20 �������F
���B���F�\����
���b�̕����y�f�ł����X���p�[�[�̓�����j�Q���A�H������̎��b�̋z����}���邱�Ƃő̏d������������
�p��Alizyme plc�����i |
�j���[���y�v�`�hY Y5��e�̝h�R��
�@velneperit |
S-2367 |
����`���� |
- |
2009/2/17 �C�OP2b�A����P2a
�V�K�^�[�Q�b�gNPY Y5��e�̂ɑ���A���^�S�j�X�g�BNPY�͐H�~��G�l���M�[�ێ�E����̃o�����X�̒����Ɋ֗^����H�~���i�`�B���q�B
���Еi |
| �@velneperit��orlistat�̔z���� |
S-2367 |
����`���� |
- |
2010�N�x�@�č�P2�������^������ڎw�� |
| �@ |
S-234462 |
����`���� |
- |
2010�N�x�@�č�P2�����J�n��ڎw��
S-2367�����ʂ̋����o�b�N�A�b�v������ |
| �V�u�g���~�����_�����a�� |
�����f�B�A/���_�N�e�B��
KES524 |
�A�{�b�g/
�G�[�U�C |
������ |
�Z���g�j������уm���A�h���i�����Ď�荞�ݑj�Q��p�Ɋ�Â��얞�ǎ��Í܁B
���E83�J���ŏ��F
2010/10/28�@�����\����艺��
2007/11/29�@�����\�� |
�A�~����/�q�g���v�`�������A�i���O
�@Pramlintide/Metreleptin |
�@ |
���c��i�H�� |
- |
2011/08/05 �J�����~
2010/02/23 �č�P3�J�n
Amylin�����i |
| �i���g���L�\�����_���������܂ƃu�v���s�I�����_���������܂̍��� |
Contrave |
Orexigen/���c��i�H�� |
- |
2011/06/03 �č��ł̊J���𒆒f
2011/02/01 �č��ɂ�����얞�ǎ��Í�ContraveR�̐R�����ʎ�́i�lj������v�j
2010/09/02 Orexigen�Ђƕ��c��i�H�ƁA�č��A�J�i�_�A���L�V�R��ΏۂƂ����Ɛ�I�J���E�̔��_������ |
| �J���i�r�m�C�h��e�̝h�R�� |
�����i�o�� |
�T�m�t�B�E�A�x���e�B�X |
- |
2008/11/5 �J�����~ |
|
|
���Z���g�j��2C��e�̂́A�H�~���ӂ��i�镪��ł��鎋���������܂߂��]�ɔ�������Ă��܂��B����������5-HT2C�ւ̎h���͐ېH�}���A�O�H�ɋ����֘A��L���Ă��܂��B |
|
�@ |
|
|
|
�@���A�_���ǂ���b�a�ԂƂ��A�ߓ��ɐ͏o�����A�_�����N���������U�����߉��Ƃ��Ĕ��ǂ��܂��B���Ǖ��ʂƂ��Ă͑��̐e�w�i��ꒆ����j�Ȃlj����������A�u�ɂɂ����s����ɂȂ�܂��B�����A�_�l���R���g���[�����������A�_���ǂ���u����ƁA�ɕ����߁A�A�H�����܂ސt��Q�ɐi�s���Ă������������ł��B�@�ɕ����҂̑�����13��9��l�i����17�N�x���Ғ����j�ƂȂ��Ă��܂����A���ۂ̊��Ґ���50�`60���l�Ɛ��肳��Ă��܂��B
�@�ɕ������A�_���ǂ̎��Ö�Ƃ��ẮA��Ƃ��ăL�T���`���I�L�V�_�[�[�i�ɕ��̌����ƂȂ�A�_�̐������y�f�j�j�Q�܂��p�����Ă��܂��B |
|
���L�T���`���I�L�V�_�[�[�F�ɕ��̌����ƂȂ�A�_���������y�f |
|
| ��ʖ� |
�u�����h�� |
�̔���� |
�������� |
���l |
�L�T���`���I�L�V�_�[�[�j�Q��
�@�A���v���m�[�� |
�U�C�����b�N |
�@ |
- |
�W�F�l���b�N�i���� |
��v�����^�I��I�L�T���`���I�L�V�_�[�[�j�Q��
�@�t�F�u�L�\�X�^�b�g |
�t�F�u���N |
��l�t�@�[�} |
- |
2011/05/13 ���{�ɂĔ���
�A���v���m�[���Ƃ͑S���قȂ��{�\����L���� |
| ���� |
ADENURIC |
�A�X�e���X���� |
- |
2010/04/01 �����E���`�ɂēƐ�̔����l��
��l�t�@�[�}�̑n���i |
| ���� |
ADENURIC |
�C�v�Z��/���i���[�j |
- |
2010/03/09 ���B�ɂĔ̔��J�n
��l�t�@�[�}����̓����i |
| ���� |
TMX-67 |
�G�X�P�[�P�~�J���Y |
- |
2010/06/30 �؍��ɂĔ̔����F�擾
��l�t�@�[�}����̓����i |
| ���� |
ULORIC |
���c��i�H�� |
- |
2009/03/13 �č��ɂĔ̔��J�n
��l�t�@�[�}����̓����i |
| ���� |
ULORIC |
���c��i�H�� |
- |
2010/10/22 �J�i�_�ɂĔ̔��J�n
��l�t�@�[�}����̓����i |
�A�_�����}����
�@�g�s���L�\�X�^�b�g |
�E���A�f�b�N |
�x�m��i/
�O�a���w������ |
- |
2013/06/28 �������F
2009/11/08 ���C�Z���X�_����� |
canakinumab�i��`�q�g�����j
�J�i�L�k�}�u |
ACZ885 |
Novartis |
- |
2011/05/25 2�̃t�F�[�YIII�̌��ʂ\ |
| �L�T���`���I�L�V�_�[�[�ƔA�_�g�����X�|�[�^�[�iURAT1�j�����ɑj�Q |
KUX-1151 |
�L�b�Z�C��i
�t�@�C�U�[ |
- |
2013/12/24 �t�@�C�U�[�Ђ֓��o |
|
|
�@ |
|
|
|
�@���e頏ǂ́A�u�����x�̒ቺ������Ƃ��A���܂̃��X�N�����債�₷���Ȃ鍜�i�����v�ƒ�`����Ă���A���ɏ����̊��җl���������߂܂��B����̐i�W�ƂƂ��ɍ��e頏NJ��Ґ��͑������Ă���A���{�����Ŗ�P�O�O�O���l�����e頏ǂł���Ɛ��肳��Ă��܂��B�Ғł��ڍ����ł̍��܂������₷���A�ꍇ�ɂ���Ă͐Q������̏�ԂɂȂ��肩�˂Ȃ����Ƃ���A���e頏ǂɑ����͈�Â݂̂Ȃ炸�Љ�I�ɂ��d�v�ȉۑ�ƋߔN�F������Ă��܂��B |
|
| ��ʖ� |
�u�����h�� |
�̔���� |
�������� |
���l |
�r�X�z�X�z�l�[�g�n
�@���Z�h�����_�i�g���E�����a�� |
�x�l�b�g |
���̑f/���c��i�H�� |
165���~
�i2012/3�j |
2012/12/25 ��1�^���܂̍������F
2010/03/16 ��1�^���܂�P3�J�n�i�����j
�C�O�ł͌�1�^���܂����F����Ă���
�ăv���N�^�[�A���h�M�����u�����n�� |
| �A�N�g�l�� |
���̑f/�G�[�U�C |
115���~
�i2011/3�j |
�r�X�z�X�z�l�[�g�n
�@�~�m�h�����_���a�� |
���J���{�� |
�����i�H�� |
9���~
�i2010/3�j |
1 ��1 �^��
2009/04/06 �������F
���{�ŏ��߂đn�ꂽ�o�����e頏ǎ��Í� |
�{�m�e�I
(�o����) |
�A�X�e���X���� |
�| |
�r�X�z�X�z�l�[�g�n
�@�~�m�h�����_���a�� |
�{�m�e�I
(�o����) |
�A�X�e���X���� |
24���~
�i2011/3�j |
���P��ԟ[�o����
2011/09/15 ��������
2010/09/10 �����\��
�A�X�e���X����̑n���A�����i�Ƌ����J�� |
| ���J���{�� |
�����i�H�� |
�| |
�r�X�z�X�z�l�[�g�n
�@�A�����h�����_�i�g���E�����a�� |
�t�H�T�}�b�N |
MSD |
�| |
�T1�^��
2010�N ���E���� 926�S��$ |
| �{�i���� |
��l�t�@�[�} |
210���~
�i2011/3�j |
�r�X�z�X�z�l�[�g��
�@�]���h�����_ |
�]���^
Zometa |
�m�o���e�B�X �t�@�[�} |
�| |
�N1��̓_�H�Ò���1�N�Ԃ̎��Â��s����B��̍��e頏ǎ��Ö�B���݊C�O90�J���ȏ�ŏ��F
2012�N ���E���� 1,288�S��$ |
| �������t�@�[�} |
�| |
2010/06/14�@���{�ɂ�����Ɛ�I�J���E�̔����錠�����擾 |
�q�g���b��B�z����������
�@�e���p���`�h�|�_�� |
�e���{���牺���p56.5��g |
�������t�@�[�} |
�| |
�T1���牺����
2011/11/25 ��������
2011/09/26 �������F
���܂̊댯���̍������e頏� |
���b��B�z����������
�i��`�q�g�����j
�@�e���p���`�h |
�t�H���e�I |
�C�[���C�����[ |
7.6���~
�i2010/12�j |
�P���P���牺����
2010/09/21 ��������
2002 �č��Ŕ����A80�ȏ�̍��ŏ��F |
�����^�r�^�~��D3����
�@�A���t�@�J���V�h�[�� |
�����A���t�@ |
��l�t�@�[�} |
114���~
�i2011/3�j |
�̑��ő�ӂ���Ċ����^�r�^�~��D3�ɂȂ�A�J���V�E���̋z���𑣐i�B�r�^�~��D�̕s���Ȃǂɂ�鍜�̕a�C�₻�̑��̏Ǐ�̉��P�A���e頏ǂ̎��Âɗp������B |
�I��I�G�X�g���Q����e�̃��W�����[�^�[�iSERM�j
�@�����L�V�t�F�� |
�G�r�X�^
(�o����) |
���O����/�C�[���C�����[ |
185���~
�i2011/12�j |
�P���P���o�����^
2011/06/03 �A�W�A7�s��̔̔����c�ɏ��n
2004/05/11 �����̔��i���O�A�����[�j
2010�N ���E���� 1,024�S��$
�o�㍜�e頏ǂ̗\�h����ю���
�C�[���C�����[���n�� |
�I��I�G�X�g���Q����e�̃��W�����[�^�[�iSERM�j
�@�o�[�h�L�V�t�F���|�_�� |
�r�r�A���g
(�o����) |
�t�@�C�U�[ |
�| |
1��1��o�����^
2010/07/23 �������F
�o�㍜�e頏ǎ��Í� |
���e頏ǂɂ������u��
�@�G���J�g�j�� |
�G���V�g�j�� |
�������t�@�[�} |
134���~
�i2011/3�j |
���e頏ǂɂ������u�� |
���S�q�g�^���m�N���[�i���R��
�@�f�m�X�}�u |
�v�����A
�牺��
6�J����1�^ |
���O�� |
�| |
2013/06/11 ��������
RANKL�ɓ��ٓI�Ɍ������A�j���זE�ɂ�鍜�j���}������BAmgen�Ђ���̓����i�B |
�r�X�t�H�X�t�H�l�[�g�n���z���}����
�@�C�o���h�����_�i�g���E�����a�� |
�{���r�oR��1mg�V�����W
�i��1�^���ˍ܁j |
���O����^�吳���� |
�| |
2013/09/29 ��������
�C�O�ł́uBonvivaR�i�č��ł�BonivaR�j�v�̔̔����Ŕ̔� |
|
|
���r�X�z�X�z�l�[�g�n�F�j���זE�ɓ����A���z����}��
����B�n�C�h���A�p�^�C�g�Ɍ������������z���Ƌ��ɔj���זE�Ɏ�荞�܂�A���z����}����B
���I��I�G�X�g���Q����e�̃��W�����[�^�[�iSERM�j�F�����������邱�Ƃō��e頏ǂ�\�h����ю��Â����܂�h���B
���q�g���b��B�z�������i�q�gPTH�j�F���`�����i��p��L����B |
|
�@ |
| �i�z��n�����j |
|
|
|
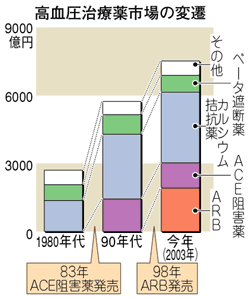
�@�����͔N��ƂƂ��㏸���A�S�O��ł͂S�l�ɂP�l�A�U�O��ł͂Q�l�ɂP�l���������ɂȂ�Ƃ���Ă���A����ɂȂ�قǍ������ɂȂ�₷���B�������͐S���a��]���Ǐ�Q�Ȃǂ̗l�X�ȕa�C�̌��ƂȂ邽�߁A���ݑ�ςɏd�v�Ȗ�ƂȂ��Ă��܂��B
�@1980�N��̍��������Ö�̓J���V�E���h�R��ƃx�[�^�Ւf��ł������A1990�N��ɂ́A����ɃA���W�I�e���V���i�`�b�d�j�ϊ��y�f�j�Q�����A���݂͂���ɃA���W�I�e���V���h�h��e�̝h�R��i�`�q�a�j���o�ꂵ�܂����B
�@���ݍł��������������ÂɎg����J���V�E���h�R��́A���ǂ��g�������p�������܂��B���p����Ƃ����Ɍ��ǂ��g������̂Ō������ቺ�B���ʂ������ɕ\��A��t���g���₷���Ƃ�������������܂��B
����ɑ��`�q�a�̓J���V�E���h�R��̂悤�ɋ}���Ɍ�����������^�C�v�̖�ł͂���܂��A�t���̕ی��p�ɗD���ȂǕ���p�͏��Ȃ��A�ق��̎��Ö�������҂Ɏ�����₷���Ƃ����Ă��܂��B���̂��ߋߔN���̃V�F�A���}���Ɋg�債�Ă��܂��B�܂��A���̓��ނ̖�܂͈�t�̔��f�ŕ��p����ꍇ�������B
�@ |
|
 |
|
�@�z�튯�p�܁A�����ǎ��Í܂̍����s���@2010�N5��6�� �x�m�o��
�@�|2018�N�̎s��\���@�~���܂P��400���~09�N��15.9�����| |
|
�@ |
|
�T�C�A�U�C�h�n���A�� �F�]���ȉ�����r������
�@���ʔA�ǂɂ����āANa�A�b���̍ċz����}�����ė��A���ʂ������܂��B�~���܂Ƃ��Ă��g�p����܂��B���A��͐t���̋@�\�P�ʂł���l�t�����̔A�ǂ�W���ǂɍ�p���A�̓��̃i�g���E���iNa�j�Ɛ����̔r���i���A�j�𑣂��A�̉t�ʁi���t�ʁj�����炷���ɂ���Č����������܂��B |
|
| ��ʖ� |
���i�� |
�̔���� |
�������� |
���l |
| �q�h���N�����`�A�W�h |
�_�C�N���g���C�h�� |
�@ |
�| |
�@ |
|
|
�@ |
|
�A���W�I�e���V���U��e�̝h�R��iARB�j �F���ǎ��k��}����
�@�A���M�I�e���V��II��e�̂́A��Ɍ��ǂ̋ؓ��ɑ��݂���^���p�N���ł��B�A���M�I�e���V��II��e�̂́A�A���M�I�e���V��II�Ƃ����^���p�N���������邱�ƂŊ���������A���ǂ����k������̂ɕK�v�ȐM�����܂��B�@
| ��ʖ� |
���i�� |
�̔���� |
�������� |
���l |
| �J���f�T���^�� �V���L�Z�`�� |
�u���v���X |
���c��i�H�� |
1,427���~
�i2012/3�j |
1999�N����
2012/3 ���E���� 2,163�S���~ |
�o���T���^��
Valsartan |
�f�B�I�o��
Diovan |
�m�o���e�B�X �t�@�[�} |
1,144���~ |
2000�N11������
2012�N ���E���� 4,417�S��$ |
| ���T���^���J���E�� |
�j���[���^�� |
MSD
�iMerck & Co., Inc.�j |
709���~ |
1998�N��s
2012�N ���E���� 1,284�S��$ |
| �I�����T���^�� ���h�L�\�~�� |
�I�����e�b�N
Benicar�i�āj
Olmetec�iEU�j |
���O�� |
823���~
�i2011/3�j |
2002�N�i�āA�Ɓj�A2004�N5���i���j����
2011/3 ���E���� 2,415�S���~
ARB�̒��ł͐��E��7�Ԗڂɏ�s���ꂽ���i |
| �e���~�T���^�� |
�~�J���f�B�X |
�A�X�e���X����
�i�x�[�����K�[�C���Q���n�C���j |
758���~
�i2011/3�j |
�x�[�����K�[�C���Q���n�C�����n��
2002�N12�� ���{����
2010�N ���E���� 1,555�S���� |
| �C���x�T���^�� |
�A�o�v��
�i2008�N�����j |
����{�Z�F����
�i�T�m�t�B�E�u���X�g���j |
107���~
�i2012/3�j |
1997�N��s
�����������������A24 ���ԍ~�����ʂ���������
2010�N ���E���� 1,176�S��$ |
�C���x�^��
�i2008�N�����j |
����`����
�i�T�m�t�B�E�u���X�g���j |
73���~
�i2011/3�j |
| �A�W���T���^���@���h�L�\�~�� |
Edarbi
�iTAK-491�j |
���c��i�H�� |
�| |
2011/12/09 �d�t�A�̔����擾
2011/04/15 �ĂŔ̔��J�n
�u���v���X�̌�p�i |
| �A�W���T���^�� |
�A�W���o |
���c��i�H�� |
�| |
2012/05/28 �����̔�
2012/01/18 �������F�擾
�u���v���X�̌�p�i |
|
|
�@ |
|
�J���V�E���h�R��iCCB�j �F���ǂ��L����
�@�J���V�E���h�R�܂͌��Ǖ����̓d�ʈˑ����ba�`�����l���ł�Ca�C�I���̍זE������}�����A�זE���V��Ca�C�I���Z�x��ቺ�����邱�Ƃɂ�茌�ǂ��g�������A�~����p�����܂��B |
|
| ��ʖ� |
���i�� |
�̔���� |
�������� |
���l |
| �A�����W�s���x�V���_�� |
�m���o�X�N |
�t�@�C�U�[ |
1,340���~ |
�������ǁE���S�ǎ��Ö�
2010�N ���E���� 1,506�S��$ |
| �A�����W�s���x�V���_�� |
�A�����W�� |
����{�Z�F����
�i�t�@�C�U�[�j |
360���~
�i2012/3�j |
���� |
| �j�t�F�W�s�� |
�A�_���[�g |
�o�C�G����i |
394���~ |
�@ |
T/L�^�J���V�E���iCa�j�h�R��
�@���_�x�j�W�s�� |
�R�j�[�� |
���a���y�L���� |
197���~
�i2011/12�j |
2011/06/02 T/L�^Ca�h�R��x�j�W�s���ƕ��p����~����͗��A�邢��ARB���]�܂��� |
| �A�[���j�W�s�� |
�J���u���b�N |
���O�� |
140���~
�i2011/3�j |
�F�����Y���n�� |
�������b���h�R�~����
�@�V���j�W�s�� |
�A�e���b�N |
���c����
���̑f���� |
141���~
�i2011/3�j |
2013/08/19 �������F�擾�i���̑f����j |
|
|
�@ |
|
���Ւf�� �F�S��������o�����t�ʂ߂���
�@�m���A�h���i�����ƃ���e�̂Ƃ̌�����j�Q���A�����_�o�̋������Ւf�����p������ł��B |
|
�@ |
|
�A���W�I�e���V���ϊ��y�f�j�Q��iACE�j
�@�A���W�I�e���V�����A���W�I�e���V��II�ɕϊ�����ACE�i�A���W�I�e���V���ϊ��y�f�Fangiotensin-converting enzyme�j��j�Q����ł��B�@�@ |
|
| ��ʖ� |
���i�� |
�̔���� |
�������� |
���l |
| �C�~�_�v�������_�� |
�^�i�g���� |
�c�ӎO�H���� |
83���~
�i2012/3�j |
1983�N���� |
|
|
�@ |
|
���ړI���j���j�Q�܁iDRI�j
�@���j���E�A���W�I�e���V���E�A���h�X�e�����E�V�X�e���iRAAS�j�̋N�_�Ɉʒu���郌�j���ړI�ɑj�Q����V������p�@��������܂ł��B
���j���͍������Ƒ����Q�������N���������ƂȂ�y�f�ł��B�@ |
|
|
|
�@ |
|
�z����
�@�������ǂ́A�����̐����ɂ�蔭�ǂ��鎾���ł��邱�Ƃ���A�~���ڕW�B���̂��߂ɂ́A��p�@���̈قȂ�~�����g�ݍ��킹�����p�Ö@���L�p�Ƃ����Ă��܂��B
�z���܂͂Q��ވȏ�̐�������̐��܂ɔz��������̂ł�����A�ʁX�ɕ��p������A���������߁A���ݖY������Ȃ����郁���b�g������܂��B
�@�܂��A�z���܂͐��@�����G�ŁA�W�F�l���b�N���[�J�[�̂ǂ��ł��ȒP�ɒǐ��ł�����̂ł͂Ȃ��̂ŁA������̐攭��Ɠ�������Ă��Ȃ����А��i��g�ݍ��킹�Ĕ̔����邱�ƂŁA���А��i�̐��i���������邱�Ƃ����݂��Ă��܂��B |
|
|
|
�@ |
|
|
|
�@���t���ɂ̓��������A�g���O���Z���h�i�������b�j�A�R���X�e���[���Ȃǂ̎��������݂��Ă��܂��B���̎����̗ʂ��ُ�ɑ�������Ԃ��u�������ǁv�Ƃ����܂��B�������ǂ��̂��̂Ɏ��o�Ǐ�͂قƂ�ǂ���܂��A�v���I�ȕa�C�ɒ��ڂȂ����Ă������߁A���߂̎��Â�\�h�͔��ɑ�ł��B
�@�R���X�e���[���́A�l�̂��\������זE����ق��A���炾�̒��q�𐮂���z��������A�H�����̎��b�̏����z����������_�`�_�̍ޗ��ƂȂ�ȂǑ�ȓ�����S���Ă��܂��B
�R���X�e���[���́A���̕��ނ���k�c�k�R���X�e���[���Ƃg�c�k�R���X�e���[���̂Q��ނɕ������A���������킹�����̂𑍃R���X�e���[���Ƃ����܂��B
����������Ƒ̂Ɉ��e�����y�ڂ��̂́A�k�c�k�R���X�e���[���ł��B���ʃR���X�e���[���Ƃ��Ă�A�̑��ō������ꂽ�R���X�e���[�����זE�ɑ��铭�������܂����A����������ƌ��Ǖǂɂ��܂�A�����d����i�߂܂��B
����A�g�c�k�R���X�e���[���́A�P�ʃR���X�e���[���Ƃ��Ă�A���Ǖǂɉߏ�ɂ��܂����R���X�e���[�����̑��ɑ��铭�������Ă��܂��B
�@�������b�́A�牺������̎��͂ɑ����A�l�Ԃ������Ă������߂̃G�l���M�[���Ƃ��Ē~�����Ă��܂��B�牺�̒������b�i�牺���b�j�ɂ́A��������g�����ۉ���p������܂��B�����̂܂��ɂ����������b�i�������b�j�́A����ؓ��A�����Ȃǂ��Ռ�������N�b�V�����̖������ʂ����Ă��܂��B���̂悤�ɁA�������b�͐l�Ԃ������Ă��������ő�Ȃ��̂Ȃ̂ł����A�]���ȃG�l���M�[�����炾�̒��ɑ���������ƁA�K�v�ȏ�ɔ牺������̂܂��Ɏ��b���~�ς���Ĕ얞�̗v���ɂȂ�܂��B
�܂��A�������b�̑����̓R���X�e���[���ɑ傫�ȉe����^���܂��B�������b�͂g�c�k�R���X�e���[�������������邽�߁A���Ǖǂ̃R���X�e���[������苎�邱�Ƃ��ł��Ȃ��Ȃ��Ă��܂��B����ɁA�k�c�k�R���X�e���[�����A��茌�Ǖǂɒ������₷�����^�Ŏ_���������̂֕ω������A�����d����i�߂����ƂȂ�܂��B
�@�������ǂ̗\�h�ɂ́A�H���̗ʂ���e���������A�^�����Ɏ������ȂǁA���C�t�X�^�C�������P���邱�Ƃ��d�v�ł��B�H���Ö@��^���Ö@���s���Ă��v���悤�Ɍ��ʂ������Ȃ��Ƃ��ɂ́A�Ö@���s���܂��B |
|
�@ |
|
�R���X�e���[���u���ʁv����ɐf�Îw�j������
�@���{�����d���w��͔]�[�ǁi���������j�⋷�S�ǂȂǓ����d���������̗\�h�⎡�ÂɎg���f�Îw�j��2007�N4���ɉ��肷��B�]���g���Ă������R���X�e���[���ɂ����u���ʁv�ƌĂ��k�c�k�R���X�e���[���������Ƃ��Ĕ��f��ɂ���B���Ղȓ��Â�}������̂��_���B�e�����銳�҂⓮���d���̗\���R�Ƃ����l��2000���l���x����Ƃ݂���B
�@2002�N�ɍ��肵�����s�w�j�͌��t1�f�V���b�g��������̑��R���X�e���[��220�~���O�����ȏ���d���ɂ���ėl�X�ȕa�C�������N�����₷���u���R���X�e���[�����ǁv�Ƃ��Ă���B��������ʃR���X�e���[������140�~���O�����ȏ�ƕύX����B
�@���R���X�e���[������ɂ���ƁA���{�l�ɑ����A�����d����h���P�ʂ́u�g�c�k�R���X�e���[���v�l�̍����l�����ÑΏۂɂȂ�A�s�v�ȓ��ÂɂȂ��鋰�ꂪ����Ǝw�E����Ă���B
�@�f�f�w�j�𓊖Â̊J�n��ƔF�����Ă����t�����邱�Ƃ���A����̒��ŁA�H�����e��։��̎w�������Â̒��S�ɂ��邱�ƂL�B��������i���Ƃ������댯���q����܂ł̒�X�N���҂́A3�`6�J���Ԏw�����Ă����P���Ȃ��ꍇ�ɓ������������Ƃ����B |
|
�@ |
|
����ɂ�镪��
| LDL�R���X�e���[���ቺ�� |
HMG-CoA�Ҍ��y�f�j�Q�܁i�X�^�`���j
�A�C�I�����������i���W���j
�t�B�u���[�g�n���
�j�R�`���_�U����
�v���v�R�[�� |
| �g���O���Z���h�ቺ�� |
�t�B�u���[�g�n���
�j�R�`���_�U����
�C�R�T�x���g�_�G�`�� |
| HDL�R���X�e���[�����グ���� |
�t�B�u���[�g�n���
�j�R�`���_�U����
HMG-CoA�Ҍ��y�f�j�Q�܁i�X�^�`���j |
|
|
�@ |
|
�X�^�`���n��iHMG-CoA�Ҍ��y�f�j�Q�܁j
�@���E�łV�܂��A100�J���ȏ�Ŕ̔�����Ă��܂��B�V�܂̔N�Ԕ���͂R���Q�牭�~�ɒB���Ă��܂��B
��ɂk�c�k�R���X�e���[����ቺ�����܂��B�̑��ł̃R���X�e���[��������j�Q���܂��B
| ��ʖ� |
�u�����h�� |
�̔���� |
�������� |
���l |
| �A�g���o�X�^�`�� |
���s�g�[��
Lipitor*
�i2001�N�j |
�t�@�C�U�[
�i�A�X�e���X�����j |
972���~
�i2011/3�j |
2012�N ���E����3,948�S��$
�������� |
| ���X�o�X�^�`���J���V�E�� |
�N���X�g�[��
Crestor
�i2006�N�j |
����`����
�i�A�X�g���[�l�J�j |
290���~
�i2011/3�j |
2012�N ���E���� 6,253�S��$
���� |
| �V���o�X�^�`�� |
���|�o�X
�i1991�N�j |
Merck & Co., Inc.
�iMSD�j |
471���~ |
�������� |
| �v���o�X�^�`���i�g���E�� |
���o���`��*
�i1989�N�j |
���O�� |
381���~
�i2011/3�j |
�E��������
�E�Ƒ������R���X�e���[������ |
| �s�^�o�X�^�`�� |
���o��
�i2003�N�j |
���a�A���Y���w
���O�� |
300���~
73���~
�i2010/3�j |
2010/07/21 ���B�ɂ�����V��̔����̏��F
2010/06/23 �č��̔��̊J�n |
| �t���o�X�^�`���i�g���E�� |
���[�R�[��
�i1998�N�j |
�m�o���e�B�X �t�@�[�}
�i�c�ӎO�H�����j |
48���~ |
����
2010�N ���E���� 436�S��$ |
|
|
�@ |
|
�t�B�u���[�g�n��
�@����̓X�^�`���n�嗬�ƂȂ��Ă��܂����A�t�B�u���[�g�n��́A�������b�̒ቺ�X�����傫���Ƃ���Ă��܂��B
��ɒ������b��ቺ�����܂��B
| ��ʖ� |
�u�����h�� |
�̔���� |
�������� |
���l |
| �x�U�t�B�u���[�g |
�x�U�g�[���r�q |
�L�b�Z�C��i�H�� |
74���~
�i2011/3�j |
�E�R���X�e���[���������}��
�E�g���O���Z���h�������}��
�E�������ǁi�Ƒ����܂ށj |
| �t�F�m�t�B�u���[�g |
���s�f�B�� |
�Ȍ�����
���������� |
42���~
�i2011/3�j |
���� |
| ��l�t�@�[�} |
�@ |
�@ |
|
|
�@ |
|
�A�C�I����������
�@��ɂk�c�k�R���X�e���[����ቺ�����܂��B
| ��ʖ� |
���i�� |
�̔���� |
�������� |
��p |
| �R���X�`�~�h |
�R���o�C�� |
�c�ӎO�H���� |
�@ |
�E�R���X�e���[���z���}��
�E�_�`�_�z���A�r�����i��p
�E���R���X�e���[������
�E�Ƒ������R���X�e���[������ |
|
|
�@ |
|
���̑�
| ��ʖ� |
�u�����h�� |
�̔���� |
�������� |
���l |
�I���K-3���b�_����
�@�I���K-3���b�_�G�`�� |
���g���K |
���c��i |
�| |
2013/01/10 ��������
Pronova Biopharma ASA�N�� |
EPA����
�@�C�R�T�y���g�_�G�`���AEPA |
�G�p�f�[�� |
���c���� |
370���~
�i2011/3�j |
���{���Y�Ƌ����J���������E���̂d�o�`���܁B�P�X�X�O�N�ɕǐ������d���ǎ��Ö�Ƃ��Ĕ����B94�N�ɂ͍������ǂ̌��\�E���ʂ��擾
�E��������
�E������ |
| �v���u�R�[�� |
�V�����X�^�[�� |
���O�� |
�@ |
�E��ɂk�c�k�R���X�e���[����ቺ������B
�E�R���X�e���[���̒_�`�_�ւ̈ى��r�����i��p
�E�������ǁi�Ƒ������R���X�e���[�����ǁA���F����܂ށj |
| �f�L�X�g�������_�i�g���E���C�I�E |
�l�c�r�R�[�� |
���a�n�� |
�@ |
�E�k�c�k�R���X�e���[���������b�����ɒቺ������B
�E�g���O���Z���h�̕��𑣐i
�E���g���O���Z���h���� |
|
|
�@ |
|
�z���� |
|
| ��ʖ� |
���i�� |
�̔���� |
�������� |
���l |
�A�����W�s���x�V���_���E�A�g���o�X�^�`���J���V�E�����a��
�i�m���o�X�N�ƃ��s�g�[���̍��܁j |
�J�f���G�b�g�z���� |
�t�@�C�U�[/�A�X�e���X���� |
�| |
2009/07/07 �������F
2010�N ���E���� 527�S��$ |
|
|
�@ |
|
|
|
�R�����͇@����n���A�A�R������A�B�R�ÌŖ��3��ނɕ��ނ���܂��B |
|
����n��� |
|
����n���͋}���S�؍[�ǁA�x�ǐ��ǂɂ����Č�����ǂ�n�������������邱�Ƃ�ړI�Ƃ��܂��B |
|
| ��ʖ� |
�u�����h�� |
�̔���� |
�������� |
���l |
| �E���L�i�[�[ |
�A�{�L�i�[�[ |
�c�ӎO�H���� |
�| |
�@ |
| �v���E���L�i�[�[ |
�v���E���L�i�[�[ |
�A�{�b�g |
- |
�@ |
| �����e�v���[�[�i��`�q�g�����j |
�N���A�N�^�[ |
�G�[�U�C |
- |
t-PA����
1998�N6��15������ |
�@ |
|
�R�������� |
|
�R�����܂́A�����̋ÏW��j�Q���܂��B��ɔ��F�����i�����Ɍ������o���₷���j�����Ȃ��悤�ɂ����p������܂ł��B�R�Ìō܂��t�B�u�����̌`����j�~���āA�ԐF�����i�Ö��Ɍ������o���₷���j��j�Q����̂Ƃ͈قȂ�A�����d�����ł̌����`����h�~���܂��B |
|
| ��ʖ� |
�u�����h�� |
�̔���� |
�������� |
���l |
| ���_�N���s�h�O���� |
�v���r�b�N�X
Plavix
�i�o���R������j |
�T�m�t�B/�u���X�g���E�}�C���[�Y �X�N�C�u |
871���~
�i2011/12�j |
2012�N ���E���� 2,066�S����
2012�N ���E����2,547�S��$
ACS���傽��K�p�B�����Ĕ]�[�ǂɓK�p
2011�N�ɉ��B�A2012�N�ɕĂœ�����
�p�i���W���̉��nj^ |
| �N���s�h�O�������_��/�A�X�s���� |
�R���v���r��R�z���� |
�T�m�t�B |
- |
2013/09/20�������F |
| �v���X�O���� |
EFIENT
�i�o���R������j |
���O��/�C�[���C�����[ |
- |
2013/06/18�����\���iACS�K�p�j
2009/02/23 ���B���F�iACS�K�p�j
2009/07/11 ����F�iACS�K�p�j
���O���ƉF�����Y������
���O���ƃC�[���C�����[�������J�� |
| �`�J�O�������iticagrelor�j |
Brilinta
�i�o���R������j |
�A�X�g���[�l�J |
- |
2010/12/06 EU�����F
2010/07/29 FDA�����F������
���l�}�����nj�Q���҂ɂ�����A�e���[�������Ǘ\�h |
| ���_�`�N���r�W�� |
�p�i���W��
�i�o���R������j |
�T�m�t�B |
- |
�@ |
| �A�X�s���� |
�o�C�A�X�s����
�i�����E���ɁE��M�܁A�R������j |
�o�C�G����i |
- |
�@ |
| ���_�T���|�O�����[�g |
�A���v���[�N
�i�����ÏW�}������і������NJg����j |
�c�ӎO�H���� |
152���~
�i2012/3�j |
���������Ǐǂɔ�����ᇁA�u�ɁA�⊴�Ȃǂ̋������Ǐ� |
| �V���X�^�]�[�� |
�v���^�[��
�i�o���R������j |
��ː��� |
528���~
�i2010/3�j |
2003�N�S���Ɂu�]�[�ǔ��nj�̍Ĕ��}���̌��\�擾 |
| �x���v���X�g�i�g���E�� |
�v���T�C����
�i���������Ǐǎ��Í��j |
�Ȍ����� |
58���~
�i2011/3�j |
���������ǏNjy�ь������x�������ǂ̎��Í� |
| ���}�v���X�g �A���t�@�f�N�X |
�I�p������
�i�����z���P���j |
�����i�H�� |
446���~
�i2010/3�j |
�ǐ��������lj��ɔ�����ᇁA�u�ɂ���ї⊴�Ȃǂ̋��������Ǐ�̉��P
��V���̍����Ғ��Nj���ǂɔ������o�Ǐ�i�����u�ɁA�������т�j����ѕ��s�\�͂̉��P |
| ���}�v���X�g �A���t�@�f�N�X |
�v�����i�[��
�i�����z���P�܁j |
����{�Z�F���� |
155���~
�i2012/3�j |
���� |
| �C�R�T�y���g�_�G�`�� |
�G�p�f�[��
�i�������ǁE�ǐ������d���ǎ����j |
���c���� |
370���~
�i2011/3�j |
���c����Ɠ��{���Y�������J�� |
| ��Ύ_�C�t�F���v���W�� |
�Z���N���[��
�i�]�z��Ӊ��P��j |
�T�m�t�B�E�A�x���e�B�X |
- |
�@ |
| �@ |
�d�T�T�T�T |
�G�[�U�C |
- |
���ĉ��Ŋe�Q�������̂o�Q�������i�s���B�`�b�r�ɂ���2012�N�x���ĉ������\����ڎw���A2010�N���߂ǂɃt�F�[�Y�V�ɒ��� |
| �@ |
K-134 |
���a |
- |
�@ |
|
|
��ACS �F �������̋������̗Տ��f�f�S�ʂ��w����I�Ȗ��̂ŁA�S�ؓ��Ŏ_�f�̎��v�Ɗ���������̋����̃o�����X�����ꂽ���ʐ�����}���S�؋����ɑΉ�����A��A�̗Տ��Ǐ���ɓ��Ă͂܂�܂��B
�s���苷�S�ǁA��ST�㏸�S�؍[�ǁi�S�d�}��ST�㏸�������Ȃ��S�؍[�ǁj����ы}���S�؍[�ǂ́A�}���̐S�؋�����悷��Տ��nj�Q�Ƃ��Ĉ�A�̕a�Ԃƍl�����Ă���A����3�ƐS���ˑR�������킹�ċ}�����nj�Q�ƌ����Ă��܂��B
���z�펾���ɂ�����R�ÌŁE�R�����Ö@�Ɋւ���K�C�h���C��
�@ |
|
�R�ÌŖ� |
|
�@�R�Ìō܂́A�Ì��̌��ɂȂ�t�B�u�����̐�����}���܂��B���t���ł܂点�Ȃ��悤�ɂ���R�����܂̒��ł��ÌŌn�ɑ��č�p������̂��R�Ìō܂ł��B��ɐÖ��̌�����x�ǐ��ɒʏ�R�ÌŖg�p����܂��B
�@�������֗^����]�S���Ǐ�Q�ɂ�鍑���̎��S�Ґ���2011�N��25���l���A����Ɏ����ő����B�����t�@�����J���E���̎s��Ƀg�����r���j�Q��Ƒ�Xa���q�j�Q�Q�����܂����B�g�����r���j�Q��͑������u���b�N�o�X�^�[�̒��ԓ�����ʂ����܂����B |
|
| ��ʖ� |
�u�����h�� |
�̔���� |
�������� |
���l |
�r�^�~��K�h�R��
�@�����t�@�����J���E�� |
���[�t�@����
(�o����) |
�G�[�U�C |
96���~
�i2011/03�j |
�r�^�~���j�̊�������j�Q���邱�Ƃɂ��C�r�^�~���j�ˑ����̋Ìň��q�̐�����}����
2010/08/30 ���m�\���F�����ǐ��ǁi�Ö������ǁA�S�؍[�ǏǁA�x�ǐ��ǁA�]�ǐ��ǁA�ɏ��ɐi�s����]�����Ǔ��j
1940�N��ɍ������ꂽ�̂��J���N���ɁA�����ł̓G�[�U�C�������ǐ��ǂ̎��ÁE�\�h��ړI��1962�i���a37�j�N�ɔ���������� |
���ڃg�����r���j�Q��
�@�_�r�K�g���� |
�v���U�L�T
(�o����) |
�x�[�����K�[�C���Q���n�C�� |
91���~
�i2011/12�j |
2011/01/21 �������F
��ٖ��ǐ��S�[�ד����҂ɂ����鋕�����]�����y�ёS�g���ǐ��ǂ̔��Ǘ}��
2010/09/20 FDA�̎���ψ�������v�ŏ��F���� |
| �g�����{���f������ �A���t�@�i��`�q�g�����j |
���R���W������
�_�H���p12800 |
�������t�@�[�} |
42���~
�i2011/03�j |
2008/04/18 �����̔�
���t�Ìőj�~��
�i�d�퐫���Ǔ��Ìŏnj�Q�iDIC�j�̎��Ö�j
|
�t�@�N�^�[Xa�i�e���G�[�j�j�Q��
�@�G�m�L�T�p���� |
���u�m�b�N�X
Lovenox
�N���L�T�� |
�T�m�t�B |
�| |
2012�N ���㍂1,893�S���� |
�I��I���ڍ�p�^��]a���q�j�Q��
�@���o�[���L�T�o�� |
�C�O�U�����g
�i�P���P��P���̌o�����^�j |
�o�C�G����i/J&J |
�| |
�K���F�ҋ@�I�G�߁E�Ҋߒu���p�������l���҂ɂ�����VTE�\�h
���E100�J���ȏ�ŏ��F |
| �o�C�G����i |
2012/01/18 ���{�ŏ��F |
���S���w������Xa�j�Q��
�@�t�H���_�p���k�N�X�i�g���E�� |
�A���N�X�g��
�i1��1��牺���^�j |
�O���N�\�E�X�~�X�N���C�� |
�| |
2011/01/21 �������F
�}���x�����ǐ��Njy�ы}���[���Ö������ǂ̎���
2010�N ���E���� 301�S���� |
�t�@�N�^�[Xa�i�e���G�[�j�j�Q��
�@�G�h�L�T�o���g�V���_�����a�� |
���N�V�A�i
(�o����) |
���O�� |
�| |
2014/01/08 ��\��
2014/01/08 ���B�\��
2011/04/22 �������F
�i�������`�O�Ȏ�p�{�s���҂ɂ�����Ö������ǐ��ǂ̔��Ǘ}���j |
�V�K�o���RFXa�j�Q��
�@�A�s�L�T�o�� |
�G���L���[�X
(�o����) |
�t�@�C�U�[
�u���X�g���E�}�C���[�Y �X�N�C�u |
�| |
2013/01/02 ����F
2012/12/25 �������F
2011/12/06 ��\��
2010/05/20 �d�t���F
�I��I�Ҋ߂Ȃ����G�ߒu���p��̐Ö������ǐ��� |
| �_���e�p���� |
�t���O�~�� |
�L�b�Z�C��i�H��/�t�@�C�U�[ |
8���~
�i2011/03�j |
�g�����{�v���X�`����}���ċÌŌn��}����
�W�F�l���b�N�i����
2010�N ���E���� 341�S��$ |
��Xa���q�j�Q��p
Otamixaban |
���p���� |
�T�m�t�B |
�| |
2013/06/03 �J�����~ |
| �t�@�N�^�[Xa�i�e���G�[�j�j�Q�� |
�_���L�T�o��
(�o����) |
�A�X�e���X���� |
�| |
2011/09/29 �J�����~ |
| �t�@�N�^�[Xa�i�e���G�[�j�j�Q�� |
TAK-442 |
���c��i�H�� |
�| |
�Ö�����ѓ������𐫍ǐ��ǎ��Ö�
2007/11/05�@�Ă���щ��B�ło�Q����
2010/10/26�@�C�OP2�����ŗL���������ꂸ |
|
|
�EFXa�j�Q�܁F���Ǔ��Ō��t�ÌłɊ֗^����FXa(���������t�Ìő�X���q)��I��I�A�t�I�����ړI�ɑj�Q����
�E�}���nj[���Ö������ǁiDVT�Fdeep vein
thrombosis�j
�E�Ö������ǐ��ǁiVTE�Fvenous thromboembolism�j |
|
�@ |
| �i��A��n�����j |
|
|
|
�@�ߊ����N���́A�~�A��Q����������Ǐ�nj�Q�ŁA�A�Ӑؔ�������i�Ƃ��A�ʏ킱��ɕp�A���ԕp�A���A�ꍇ�ɂ���Ă͐ؔ����A���ւ��܂��B�g�C���̕s���̂��߂ɊO�o���T������A��Ԃ̐������[���Ɏ��Ȃ�������Ɠ��X�̍s������������A���҂�QOL
���������ቺ���Ă��܂����Ƃ�OAB �̑傫�Ȗ��ƂȂ��Ă��܂��B
�@���{�r�A�@�\�w��̉u�w�����ɂ��ƁA40
�Έȏ�̒j���S�̂�12.4���A��810 ���l�����{�ɂ�����ߊ����N���̐��݊��҂ł���Ɛ��肳��Ă��܂��B���݁A�ߊ����N�����Ö�s���340���~���x�ł����A4�C5�N���600���~�Ɋg�傷��Ɨ\������Ă��܂��B |
|
�@ |
|
|
|
�@ |
|
|
|
�A���o�ɂ����i�r�A����A�A�������A�A���o��������i�p�A�j�A�A���o�鎞�ɒɂ��i�r�A���Ɂj�Ƃ������Ǐ�́A�r�A��Q�Ƃ��Ă܂Ƃ߂��܂��B
�@�A���o�ɂ����A�p�A������Ƃ����ꍇ�́A����j���ł͑O���B���ǁA���邢���N�����x�z���Ă���_�o�Ɉُ킪����_�o�����N�����l�����܂��B |
|
�@ |
|
| ��ʖ� |
�u�����h�� |
�̔���� |
�������� |
���l |
�O���B���ǂɔ����r�A��Q���P��
�@���_�^���X���V�� |
�n���i�[�� |
�A�X�e���X���� |
296���~
�i2011/3�j |
2010/3 ���E���� 1,139���~ |
�O���B���ǂɔ����r�A��Q���P��
�@�V���h�V�� |
�����[�t |
�L�b�Z�C��i�H��
���O�� |
97���~
101���~
�i2011/3�j |
�@ |
�O���B���ǂɔ����r�A��Q���P��
�@�i�t�g�s�W�� |
�t���o�X |
�������t�@�[�} |
139���~
�i2011/3�j |
2007/07/27 ��������
BPH�̔��ǂɊ֗^���Ă���O���B�E�A�������̃�1��e�̂��Ւf���邱�Ƃ��O���B�̎��k��}�������郿1��e�̎Ւf�� |
�_�o�����N�����P��
�@�v���s�x�������_�� |
�o�b�v�t�H�[ |
��Q��i�H�� |
70���~
�i2011/3�j |
�A���ցE�p�A���Í� |
�_�o�����N�����P��
�@���_�I�L�V�u�`�j�� |
�|���L�X |
�T�m�t�B�E�A�x���e�B�X |
�| |
�@ |
|
|
�@ |
| �i�ċz��n�����j |
|
|
|
�ȑO�́A�u�x�C��v�ƌĂ�Ă��������Ɓu�����C�ǎx���v�ƌĂ�Ă��������́A�����ǐ��x�����iCOPD)�Ƃ��đ��̂���悤�ɂȂ�܂����B
�����ǐ��x�����́A���E��2��1000���l�̊��҂��늳���Ă���A2020�N�܂łɎ��S�����̑�3�ʂɂȂ�Ɨ\������Ă��܂��B���̏Ǐd��ȏ�Q�������N�������߁ACOPD�́A���Җ{�l�A�Ƒ��A�Ђ��Ă͎Љ�S�̂ɐ[���ȉe����^���Ă��܂��BCOPD�����S�Ɏ��������邱�Ƃ͂ł��܂��A�K�Ȏ��Âɂ���ďǏ���Ǘ����邱�Ƃ��\�ł���A�����f�f�ƌ��ʓI�Ȏ��Â��d�v�ł��BCOPD�̍ő匴���͋i���ł��B |
|
| ��ʖ� |
�u�����h�� |
�̔���� |
�������� |
���l |
ICS/LABA�z����
�@�t���`�J�]���t�����J���{���_�G�X�e��/�r�����e���[���iFF/VI�j |
�����x�AR�G���v�^R
������z���� |
�O���N�\�E�X�~�X�N���C���ATheravance |
- |
2013/09/20 �������F
2013/05/10 ����F
COPD�A�C�ǎx�b�����Ö�
COPD�A�C�ǎx�b�����Ö�
���B�@�C�ǎx�b��/COPD�̓K���\���� |
LAMA/LABA����
�C���_�J�e���[���}���C���_���^�O���R�s���j�E���L���� |
�E���e�B�u��R�z���p�J�v�Z��
������z���� |
�m�o���e�B�X �t�@�[�} |
- |
2013/09/20 �������F
2012/10 ���B�\���A�č��ł�2014�N�̐\����\��
���[�����O���[�v���瓱��
COPD���� |
LAMA
�@tiotropium
�@�`�I�g���s�E���L���� |
Spiriva
�X�s���[�o
�������z���� |
�x�[�����K�[�C���Q���n�C��/�t�@�C�U�[ |
�s�� |
���ۓI�ȃK�C�h���C����COPD�̑�1�I���ɐ����B�ł��L����������Ă���
2011�N ���E���� 3,100�S����
2004�N�@���{����
2002�N�@���Ĕ���
�x�[�����K�[�C���Q���n�C���N�� |
LAMA
�i�����ԍ�p�����X�J�����h�R��j
�@�O���R�s���j�E���L���� |
�V�[�u��
Seebri Breezhaler
������z���� |
�m�o���e�B�X �t�@�[�} |
- |
2012/10/01�@EU���F
2012/09/28�@�������F
�G�[�U�C�Ƌ����v�����[�V����
2014 ��\���\��
COPD����
�x�N�`�����ЁA���[�����O���[�v�N�� |
LABA
�i��2�A�h���i������e�̎h���܁j
�@�T�����e���[���L�V�i�z�_�� |
�Z���x���g |
�O���N�\�E�X�~�X�N���C�� |
�s�� |
2010�N ���E���� 201�S�����@ |
LABA
�@�z�����e���[���t�}���_�����a�� |
�I�[�L�V�X
�������z���� |
�A�X�g���[�l�J
Meiji Seika �t�@���} |
- |
2012/09/03�@�������� |
LABA
�����ԍ�p���z���C�ǎx�g����
�@�C���_�J�e���[���}���C���_�� |
�I���u���X
Onbrez Breezhaler
�J�v�Z��150 ��g
�������z���� |
�m�o���e�B�X �t�@�[�} |
- |
2011/11/18�@�G�[�U�C�Ƌ����v�����[�V�����_��̒���
2010/09/20�@��������
OnbrezR BreezhalerR�̐��i���ŁA���B�A���iEU�j�A�X�C�X�A�I�[�X�g���A���͂��ߐ��E30�J���ȏ�ŏ��F����Ă���i2010�N7�����݁j
COPD���� |
LABA/�X�e���C�h������
�@�T�����e���[���L�V�i�z�_�� / �t���`�J�]���v���s�I���_�G�X�e��
�i�t���^�C�h�ɃZ���x���g�iLABA�j�����������܁j |
�A�h�G�A |
�O���N�\�E�X�~�X�N���C�� |
�s�� |
2010/04/23 �@�����̔�
2010�N ���E���� 5,139�S����
COPD�A�C�ǎx�b�����Ö� |
LABA/�X�e���C�h������
�@�z�����e���[���t�}���_�����a��/�u�f�\�j�h�i�p���~�R�[�g���I�[�L�V�X�iLABA�j�����������܁j |
�V���r�R�[�g
1��2���z���� |
�A�X�g���[�l�J |
- |
2010/01/13 ��������
2000�N�ɉ��B�ŏ��߂ď��F
COPD�A�C�ǎx�b�����Ö� |
�I��I�z�X�z�W�G�X�e���[�[�iPDE�j-�W�j�Q��
�@���t���~���X�g |
Daliresp
�_�N�T�X�i���EEU�j
������o���� |
Nycomed
�i���c��i�H���j |
������ |
2011/03/01 �@FDA���F
COPD���� |
�Z���ԍ�p����2�A�h���i������e�̎h����/�R�R����������
�i�C�ǎx�g����j
�@���_�T���u�^���[�E�C�v���g���s�E���L���� |
�R���r�x���g�z���� |
�x�[�����K�[�C���Q���n�C�� |
������ |
2010�N ���E���� 727�S����
�C�ǎx�b�����Ö� |
LABA
�@�N�����u�e���[�����_�� |
�X�s���y���g |
��l�t�@�[�} |
- |
�C�ǎx�b�����Ö� |
�R�R������
�i�C�ǎx���k�}���܁j
�@�C�v���g���s�E���L�������a�� |
�A�g���x ���g |
��l�t�@�[�} |
- |
2010�N ���E���� 804�S����
�C�ǎx�b���A�����C�ǎx�����Ö�
�x�[�����K�[�C���Q���n�C���N�� |
�z���X�e���C�h�b������
�@�V�N���\�j�h |
�I���x�X�R |
��l�t�@�[�} |
- |
�C�ǎx�b�����Ö� |
�z���X�e���C�h��
�@�v���s�I���_�t���`�J�]�� |
�t���^�C�h
Flixotide/Flovent |
�O���N�\�E�X�~�X�N���C�� |
�s�� |
�C�ǎx�b�����Ö� |
�z���X�e���C�h��
�@�u�f�\�j�hBudesonide |
�p���~�R�[�g |
�A�X�g���[�l�J |
�s�� |
�C�ǎx�b�����Ö� |
LAMA/LABA����
�E���N���W�j�E��/�r�����e���[��
�iUMEC/VI�j |
������z���� |
�O���N�\�E�X�~�X�N���C���ATheravance |
- |
2013/04/23�@�����\��
2013/01/10�@���B���F�\��
2012/12/18�@����F�\��
COPD���� |
��2�A�h���i�����E���Z�v�^�[�쓮��
�@�x�h���h���� |
MN-221 |
Medicinova, Inc. |
- |
2011/08/24 �t�F�[�Y1b�������^�Տ���������
�L�b�Z�C��i�H�Ɗ�����Ђ��n��
COPD���� |
�����ԍ�p�^�C�ǎx�g����
�@Aclidinium
�@�A�N���W�j�E���L���� |
KRP-AB1102
�i�z���܁j |
�L���[�������� |
- |
�Տ�����������
2011/02/24 ���C�Z���X�_��
�A���~���[���Ёi�X�y�C���j�N��
COPD���� |
LABA/�z���X�e���C�h������
�@�t���`�J�]���v���s�I���_�G�X�e��
�����ԍ�p����2 �h����
�@�z�����e���[���t�}���_�����a�� |
KRP�]108
��ʕ������z���� |
�L���[�������� |
- |
2012/09/25 �������F�\��
SkyePharma PLC�N��
�C�ǎx�b�����Ö� |
�����ԍ�p�^�R�R�������C�ǎx�g����
�@�`�I�g���s�E�� |
1��1���z���� |
�x�[�����K�[�C���Q���n�C�� |
- |
2012/09/03 P3����
�C�ǎx�b�����Ö� |
| CRTh2��PGD2�̌�����j�Q |
ADC3680 |
��l�t�@�[�} |
- |
2012/09/26 �Ɛ�I�J���������̔��_������
�v���}�W�F���Ёi�p���j�N��
�C�ǎx�b�����Ö� |
|
|
���@LAMA�F������p�����X�J�����h�R�܁iLong-Acting Muscarinic Antagonist�j
�@�@ LABA�F�����ԍ�p�^��2�쓮��iLong-Acting
Beta2 Agonist�j
�@�@ ICS�F�z���R���`�R�X�e���C�h�iInhale
corticosteroid�j
|
|
�@ |
|
|
|
�@�Ԏ����x���Ƃ́A�x�̊Ԏ��i�x�̋�C�����镔���ł���x�E�������������ŁA��ɔx���x���������S���Ă��܂��j�𒆐S�ɉ��ǂ𗈂������̑��̂ł��B
�@�ۂȂǂ̊������Ȃ��ɂ�������炸�A���炩�̌����ŁA�x�̒��́u�Ԏ��v�Ƃ��������ɁA�����I�ɉ��ǂ��N����a�C�ł��B�Ԏ��́A�C�ǎx�̐�[�ɂ���x�E�Ɣx�E�̊Ԃɂ���g�D�̂��ƂŁA���ǂɂ��A�d���A�����Ȃ��Ă����܂��B���̂��߁A�Ԏ����x���ł́A�x�S�̂��d���Ȃ�A�L����ɂ����Ȃ��āA�����\���ɋz�����߂Ȃ��Ȃ�̂ł��B60�Έȏ�̍���̒j���ŁA�i�����Ă���l�ɑ������ǂ��A3�`4�N�����Ă������Ɛi�s����a�C�ł��B�������x���ۏǁi�P�ɔx���ۏǂƂ������j�ȂǑ��l�ȕa�^���܂�ł��܂����A���̑����͌������s���ł���A�܂����Â�����Ȏ����ł��B |
|
| ��ʖ� |
�u�����h�� |
�̔���� |
�������� |
���l |
�R���ۉ���
�@�s���t�F�j�h�� |
�s���X�p |
����`���� |
28���~
�i2011/3�j |
2008/10/16�@�������x���ۏǎ��Ö�̐����̔����F�擾 |
|
|
���������x���ۏǁF�����s���̎����ł���A�x�E�ǂ̐��ۉ����i�s���邱�Ƃɂ��A�s�t���̖I���x�i������\CT
�ɂĔx���I�̑��l�Ɏʂ��ԁj�`�����������\��s�ǂ̎����ł��B��ʓI�ɍS������Q�k�x���ʂ�S�x�C�ʂ̌����l���F�߂��܂��B�Ǐ�i�x�E�ǂ̐��ۉ��j���i�s����Ɣx�ł̃K�X�����i�_�f�Ɠ�_���Y�f�̌����j������ɂȂ�_�f�z���Ö@�����K�v�ɂȂ�ꍇ������܂��B���Y�����́A�d�Ǔx�ɂ���ẮA���莾���i�������a�j�Ɏw�肳��Ă��܂��B |
|
�@ |
|
|
|
�@�C���t���G���U�E�C���X�͌��X���Ȃǒ��ނ̒����E�C���X���N���ł���A���������A�q����j���g���Ȃǂ̉Ƌׂ���A�ʏ�u�^����Đl�Ɋ����v���܂��B�����͂���ϋ����A�����ɂ���������1�`2�����o�Ĕ��a�A�ቷ�E�Ꮌ�x�̓~�G�ɑ嗬�s���܂��B
�@���I�̎l�嗬�s�Ƃ�������̂ɁA1918�`1919�@�X�y�C�������A1957�`1958�@�A�W�A�����A1968�`1969�@���`�����A1977�`1978�̃\�A����������A���̂����A�X�y�C�����ׂ́A6���̐l�����A2300���l�����S�A�킪���ł��l���̔����߂������A38���l���S���Ȃ�܂����B�l�X���Ɖu�������Ȃ��V�^�C���t���G���U����������ƁA���̂悤�Ɉ�勺�ЂƂȂ�܂��B
�@�C���t���G���U�ɂ́A�E�C���X�\�ʓˋN�̍R�����̈Ⴂ�ɂ��A�^�AB�^�AC>�^������܂��BC�^�́A�H�ɏ������ɏd�lj����邱�Ƃ�����܂����A���l�ł͏Ǐy���A������ɂ����܂���ɂȂ�܂���B �C���t���G���U�i���ɂa�^�j�́A��N�҂ɑ�����������X��������܂��B
�@ �z�튯�p�܂Ɗ����ǎ��Í܂̍����s��� 2008�N4��11�� �x�m�o��
�@�|�\�h�ڎ�̑����Ƃ���\�h�Ŏs��g�傪���҂���郏�N�`�����܁|�@ |
|
�@ |
|
20���I�ɑ嗬�s�����V�^�C���t���G���U |
|
|
|
�@ |
|
�G�ߐ��C���t���G���U |
|
�G�ߐ��E�C���X�ɂ́u�`�\�A�^�v�u�`���`�^�v�u�a�^�v�̂R��ނ�����܂��B���{�ł͔N��1���l�O�オ���S�B�ߔN�̎��S�҂̂W���ȏ��65�Έȏ�̍���҂ł��B�č��ł͖��N���ς��Ė�R���U�O�O�O�l���A�ʏ�̃C���t���G���U�ɂ�莀�S�B�S���E�ł͂��̐��́A����łQ�T���T�O���l�ɒB����Ƃ����Ă��܂��B |
|
�@ |
|
| ��ʖ� |
�u�����h�� |
�̔���� |
�������� |
���l |
�m�C���~�j�_�[�[�j�Q��
�@�I�Z���^�~�r�� |
�^�~�t���E���� |
���O���� |
87���~
�i2011/12�j |
���\�E���ʁFA�^����B�^�C���t���G���U�E�C���X�����ǂ̎��� |
�m�C���~�j�_�[�[�j�Q��
�@�U�i�~�r�� |
�������U�E�z�� |
�O���N�\�E�X�~�X�N���C�� |
- |
���\�E���ʁFA�^����B�^�C���t���G���U�E�C���X�����ǂ̎���
2010�N ���E���� 121�S�����@ |
| �@�A�}���^�W�� |
�V�����g�����E���� |
�m�o���e�B�X �t�@�[�} |
- |
���\�E���ʁFA�^�C���t���G���U�E�C���X�����ǂ̎��� |
�m�C���~�j�_�[�[�j�Q��
�@�y���~�r�����a�� |
���s�A�N�^
�i�_�H���p�j |
����`���� |
3���~
�i2011/3�j |
2010/01/26 ��������
���\�E���ʁFA�^����B�^�C���t���G���U�E�C���X�����ǂ̎���
�{�܂ɂ�鎡�Â�1��Ŋ��� |
�����ԍ�p�^�m�C���~�j�_�[�[�j�Q��
�@���j�i�~�r���I�N�^���_�G�X�e�����a�� |
�C�i�r���z��������20�r |
���O�� |
66���~
�i2011/3�j |
2012/08/22 P3�����i�C���t���G���U�E�C���X�����Ǘ\�h�j����
2010/09/10 �������F�i2010/10/19 ���������j
���\�E���ʁFA�^����B�^�C���t���G���U�E�C���X�����ǂ̎���
�{�܂ɂ�鎡�Â�1��Ŋ���
�I�Z���^�~�r����5���ԓ��^�Ɠ����̌��ʂ����� |
�E�C���X�R��RNA�|�������[�[�j�Q��
�@�t�@�r�s���r�� |
T-705 |
�x�R���w�H�� |
- |
2011/03/30 �����\��
2010/02/15 �č��ł̗Տ���II���������J�n
�E�C���X�\�ʓˋN�̍R�����̈Ⴂ�Ɉˑ����Ȃ����߁AH5N1�^���܂ލL�͈͂ȃC���t���G���U���^�[�Q�b�g�Ƃ���B |
Specific anti-H5N1 polyclonal immunoglobulins
�i�E�C���X�𒆘a���鍂���x�̖Ɖu�O���u�����j |
�E�C���X��F���E�W�I���E���a�ł�������^�R�́i�Ɖu�O���u�����j�����҂ɒ��� |
Fab�fentech |
- |
2012/10/11 ��1���Տ��������V���K�|�[���ŊJ�n |
|
|
��RNA�|�������[�[
�l�Ԃ̍זE�Ń^���p�N�������������ߒ��̏o���_��DNA�ŁARNA�|�������[�[�ɂ��DNA�̏��RNA�ɓ]�ʂ���A���̏������ƂɃ^���p�N���������܂��B |
|
�@ |
|
�v���p���f�~�b�N���N�`�� |
|
�@�u�V�^�C���t���G���U�p�̃��N�`���v�́A�V�^�C���t���G���U�E�C���X���������Ȃ��Ɛ������邱�Ƃ��ł��܂���B�����_�ł́A�V�^�C���t���G���U�E�C���X�����݂��Ȃ����߁A���N�`��������܂���B�������A���{���܂ސ�i�H�ƍ��ł́A����܂ł̒�����q�g�֊����������Ⴉ�番�����ꂽ�E�C���X�����Ƀ��N�`���p�ɊJ�����ꂽ��E�C���X����AA/H5N1���^�̃C���t���G���U�E�C���X�ɑ��郏�N�`�����J�����Ă��܂��B���̃��N�`���́u�v���p���f�~�b�N���N�`���v�Ƃ����ʒu�Â��ɂȂ�A�V�^�C���t���G���U�p�̃��N�`���ł͂���܂���B
�@���ۂɂ̓p���f�~�b�N�ɂȂ����ۂɁA���̂Ƃ��̃E�C���X���g�p���Đ��������u�p���f�~�b�N���N�`���v���K�v�ƂȂ�܂��B
�@�������Ȃ���A�p���f�~�b�N���N�`���͂����܂Ńp���f�~�b�N���������Ă���łȂ��Ɛ����ł��܂��A���̐����ɂ́A�E�C���X����������Ă��班�Ȃ��Ƃ��U�J���Ԃ�����܂��B���̂��߁A�ŏ��̃p���f�~�b�N���g�ɂ͊Ԃɍ���Ȃ��̂ŁA�ɂ���ẮA���Ȃ��Ƃ���b�Ɖu�����邱�Ƃ��ł���u�v���p���f�~�b�N���N�`���v��ڎ킷�邱�Ƃ��l�����Ă��܂��B�@ |
|
|
|
�@ |
|
���{�̃��N�`�����|�J�[ |
|
|
|
�@ |
|
�p����� |
|
�m�C���~�j�_�[�[
�@�m�C���~�j�_�[�[�iNA�j�́A�E�C���X�\�ʂɂ���ˋN�̂��ƂŁANA�́A���̓��ɐN�������E�C���X���W�I�זE�ɓ��B����O�ɃV�A���_���܂ޑj�Q���q�ŕs��������邱�Ƃ�h���܂��B�܂��ANA�͊����זE���ő��B�����E�C���X���q���A�����זE������o����ۂɓ����܂��B���̓����ɂ���ăE�C���X�́A�������̍זE�ւƎ���ɍL�����Ă����A����Ȃ鑝�B���\�ɂȂ�܂��B�m�C���~�j�_�[�[�j�Q�܂͂��̓������~�߂邱�ƂŁA�C���t���G���U�E�C���X�̑��B��}���܂��B���{�����ŏ��F����Ă���m�C���~�j�_�[�[�j�Q�܂ɂ́A�U�i�~�r������_�I�Z���^�~�r��������܂��B
�@���݁A�m�C���~�j�_�[�[��A�^�C���t���G���U�E�C���X�ɂ�����9��ނ�����Ă���A�q�g�Ɋ�������C���t���G���U�E�C���X�ł�N1�AN2��2��ނ��킩���Ă��܂��B���̑��A�u�^�iN2�AN3�j�A�E�}�iN7�AN8�j�A�A�U���V�iN6�AN8�j�ɂ��āA2��ނ��m�F����Ă��܂����A���ނ�9��ޑS�ẴP�[�X������Ă��܂��B
�@ |
RNA�|�������[�[
�@DNA�𒒌^�Ƃ��� RNA ����������y�f�Łu�]�ʍy�f�v�Ƃ��Ă��B���m�ɂ́uDNA �ˑ��� RNA �|�������[�[�v�Ƃ����A����ނ̃^���p�N���i�T�u���j�b�g�j����\�������^���p�N�����̂ł���B�^���p�N���̐v�}�͈�`�qDNA�ɑ��݂��邪�A��`�q�ɏ����ꂽ�^���p�N���̏��i����z��j�͂�������mRNA(���b�Z���W���[RNA)�ɓ]�ʂ��ꂽ��ɁA���{�\�[���ɂ���ăA�~�m�_�ւƖ|��^���p�N�����ł���B������DNA����mRNA�ւ̓]�ʂ��s���̂�RNA�|�������[�[�ł���BRNA�|�������[�[�͈�`�qDNA�𒒌^�ɁARNA�̑f�ƂȂ�4�̃k�N���I�V�h�iA�F�A�f�m�V��,
U�F�E���W��, G�F�O�A�m�V��, C�F�V�`�W��)���d����mRNA����������B
�@�܂����^��K�v�Ƃ��Ȃ��y�f������A�^�j�����̂���poly(A) �|�������[�[�́A���^��K�v�Ƃ��Ȃ��ŋt�]�ʎY����poly(A) ����t�����邱�Ƃœ]�ʌ�̈�`�q��������@�\�������Ă���B����𒒌^��ˑ����q�m�`�|�������[�[�Ƃ����B
�@ |
���a�������C���t���G���U
�@���a�������C���t���G���U�Ƃ́A���ނ̂����j���g���Ȃǂ̉Ƌחނɍ��v�����̕a�����������C���t���G���U�E�C���X�����ɂ�鎾�a�ŁA�Ƌחނ���������ƁA�_�o�Ǐ�A�ċz��Ǐ�A������Ǐ̑S�g�Ǐ���������܂��B�܂��A����܂łɎ�ł̃C���t���G���U�E�C���X���Ƌחނœ`�d���J��Ԃ������ɁA���łɕψق���������m�F����Ă��܂��B1997�N�ɍ��`�Ŕ����������a�������C���t���G���U�E�C���X�����ɂ��18�l��6�l���S�̏Ǘ�ȗ��A�ƋחނɌ��炸�A�d�v�Ȑl�b���ʊ����ǂƔF������Ă��܂��B
�@ |
H5N1�^�g���C���t���G���U�E�C���X
�@A�^�C���t���G���U�E�B���X�̈��ł���A���a�����g���C���t���G���U�̌����ƂȂ�E�B���X�B
�����͂ɂ���߂ĕx�ގ�ނł���A���ނ����łȂ��l�ɂ���������B ���ݐl����l�ւ͊������Ȃ������̃E�B���X�͕ψق��ĐV�^�C���t���G���U�E�B���X�ɂȂ�\���������ƌ����Ă���AWHO���x�����Ă���B
�@���܂ł̃C���t���G���U�E�B���X�͌ċz��̕\�w�̉��ǂ����ōς�ł��邪�A���̃E�B���X�͌��t����đ��̓����ɂ����ǂ������N��������d�ēx�̍����댯�ȃE�B���X�ł���B |
|
|
�@ |
| �i������n�����j |
|
|
|
�ߔN�H���̉��ĉ����i�ݑ����Ă��܂����B�ݎ_���t�����āA�H���̔S���������邱�Ƃɂ���āA�u���₯�v��A�̂ǂ̈�a���A�����Ղ��������Ă���Ȃǂ̏Ǐo�܂��B���Ăł͐��l�̖�40�����A���{�ł�20���߂����t�����H�����ł͂Ȃ����Ɛ�������Ă��܂��B |
|
| ��ʖ� |
���i�� |
�̔���� |
�������� |
���l |
�v���g���|���v�j�Q�܁iPPI�j
�@�����\�v���]�[�� |
�^�P�v���� |
���c��i�H�� |
765���~
�i2012/3�j |
2012/03 ���E���� 1,221���~
�ݔS���̃v���g���|���v�̍y�f������j�Q���邱�Ƃɂ���āA�ݎ_�̕����}���B�݁E�\��w����ᇁA�t�����H�����A��т�ݐH���t���ǂȂǂ̎��ÁB |
�v���g���|���v�j�Q�܁iPPI�j
�@���x�v���]�[���i�g���E�� |
�o���G�b�g |
�G�[�U�C |
602���~
�i2011/3�j |
2011�N ���E���� 1,369���~
�ݒ�ᇁA�\��w����ᇁA��������ᇁA�y�����������������|�d�������������nj�Q�̎��ÁB�t�����H�����̎��ÁB |
�v���g���|���v�j�Q�܁iPPI�j
�@�G�\���v���]�[���}�O�l�V�E�����a�� |
�l�L�V�E��
�i1��1�^�j |
�A�X�g���[�l�J/���O���i���ʁE�̔��j |
�| |
2011/09/15 ��������
2010/10/29 ���O���ƃR�E�v�����[�V�����_��
���E�ōł�����Ă���PPI�B
2010�N ���E���� 4,969�S��$
�A�X�g���[�l�J�N���B�I���v���]�[���̌��w������ |
�v���g���|���v�j�Q�܁iPPI�j
�@�I���v���]�[�� |
�I���v���[�� |
�A�X�g���[�l�J |
�| |
�@ |
�v���g���|���v�j�Q�܁iPPI�j
�@�I���v���]�[�� |
�I���v���]�� |
�c�ӎO�H���� |
48���~
�i2011/3�j |
�@ |
| �@���T�v���h�N�G���_�����a�� |
�K�X���`�� |
����{�Z�F���� |
212���~
�i2012/3�j |
�ݒ��ǐ_�o�ɓ����Ĉݒ��̉^���������ɂ��A�f���C�A�q�f�A�H�~�s�U�A�c�����A���₯�Ȃǂ̏Ǐ�����P����B |
| �J���E���C�I�������^�A�V�b�h�u���b�J�[�iP-CAB�j |
TAK-438 |
���c��i�H�� |
�| |
2014/03/27 ��ː���ƍ��������v�����[�V�����_������
2014/02/28 �����\��
�����̂o�o�h���܂Ɣ�r���ċ��͂Ȉݎ_����}����p�A�Z���Ԃł̍�p�����A�����Ԃ̍�p�����Ȃǂ̓_�ŏ�����ʂ����ҁB |
|
|
�@ |
|
|
|
�@���^�E�C���X�ݒ����́A���^�E�C���X�̊����ɂ���Ĉ����N�������ݒ����ł���A���E����5�Έȉ��̏����̖�95�������^�E�C���X�Ɋ������Ă��܂��B��ȏǏ�͌�����������q�f�ŁA�d�lj�����ƒE���Ǐ�⍇���ǂ��玀�ɂ����邱�Ƃ�����A���E�ł̔N�Ԏ��S�Ґ���60���l�ȏ�Ɛ��肳��A���S��̑����́A�A�t���J�A�C���h���嗤�A����у��e���A�����J�Ȃǂ̓r�㍑�Ŕ������Ă��܂��B
�@��Â��[�����Ă�����{�ł̎��S��͏��Ȃ����̂́A�N�Ԗ�80���l�̓��c���������O������f���A��7��8,000�l��5�Ζ����̏��������@���Ă���Ɛ��肳��Ă��܂��B |
|
| ��ʖ� |
�u�����h�� |
�̔���� |
�������� |
���l |
| ���^�E�C���X�ݒ����\�h���N�`�� |
Rotarix
(�o����) |
�O���N�\�E�X�~�X�N���C�� |
������ |
2009/11/27�@�������F�\��
2��ڎ�̌o�����N�`��
���� �A���c����Ώۂɓ����������܂��邢�͉t�܂Ƃ��Đ��E116�����ŏ��F����Ă���B
2010�N ���E���� 235�S���� |
| 5���o�������^�E�C���X���N�`�� |
RotaTeq
(�o����) |
MSD |
- |
2010/03/31�@�������F�\��
�o���̐����N�`��
2006�N�č��ŁuRotaTeq�v�̐��i���ŏ��F����A����܂łɐ��E90�ȏ�̍��܂��͒n��ŏ��F����Ă���B |
|
|
�@ |
|
|
|
�@���݁A���{�ł͖�150 ���`200 ���l�̂b�^�̉��E�C���X�����҂�����Ɛ��肳��A�܂��̍זE�����҂̖�80���͂b�^�̉��E�C���X�̊����҂ł��邱�Ƃ��킩���Ă��܂��B
�@�b�^�����̉��̍����Ö@�Ƃ��ăC���^�[�t�F�������܂��L���p�����Ă���A���̎g�p�ɂ������Ă͌����J���Ȃ���u�̍d�ς��܂߂��E�C���X���̎������Â̕W�����Ɋւ���K�C�h���C��2009�v��������A���Ɣ��f���ꂽ�Ǘ�ɑ��ẮA�y�O�C���^�[�t�F����
�A���t�@���܂ƃ��o�r�����Ƃ̕��p�Ö@����������Ă��܂��B
�@�������ۈ�ÃZ���^�[ �̉����Z���^�[
�@ |
|
| ��ʖ� |
�u�����h�� |
�̔���� |
�������� |
���l |
�i�V�R�^�j
�C���^�[�t�F���� �x�[�^���� |
�t�G���� |
����/���O�� |
- |
1985�N���̔����J�n�����������̃C���^�[�t�F�������� |
�i�V�R�^�j
�C���^�[�t�F�����[������ |
�X�~�t�F���� |
����{�Z�F���� |
51���~
�i2011/3�j |
�@ |
�i��`�q�g�����j
�C���^�[�t�F�����A���t�@�R���|�P |
�A�h�o�t�F���� |
�A�X�e���X���� |
- |
�@ |
�i��`�q�g�����j
�y�O�C���^�[�t�F���� �A���t�@�|�Q�� |
�y�K�V�X |
���O����/���V�� |
83���~
�i2011/12�j |
2010�N ���E���� 1,645�S��CHF |
| �y�O�C���^�[�t�F������-2�� |
�y�O�C���g���� |
Merck & Co., Inc.
MSD |
- |
2010�N ���E���� 737�S��$�@ |
�R�E�C���X��
�@���o�r���� |
���x�g�[�� |
Merck & Co., Inc.
MSD |
- |
�y�O���C���^�[�t�F�������p�Ö@�Ŏg�p
2010�N ���E���� 221�S��$ |
NS3-4A�v���e�A�[�[�j�Q��
�@Telaprevir�i�e���v���r���j
�i��ꐢ��j |
INCIVEK
(�o����) |
���@�[�e�b�N�X
�c�ӎO�H���� |
14���~
�i2012/3�j |
2011/09/26 �������F
2011/05/23 �e�c�`�����F
�C���^�[�t�F������R���̃W�F�m�^�C�v1
HCV
RNA�E�C���X�����͂ɗ}������o�����^���\�Ȏ��Ö�
�ă��@�[�e�b�N�X�ЋN�� |
�e���r�b�NR��250mg
(�o����) |
C�^�̉��v���e�A�[�[�j�Q��
�@boceprevir�i�{�Z�v���r���j
�i����j |
VICTRELIS
(�o����) |
Merck & Co., Inc. |
������ |
2011/05/20 EU�����F����
2011/05/17 Roche�ЂƋ����̔��ō���
2011/05/13 �e�c�`�����F |
����
�@ABT-450/r, ABT-267, ABT-333
and ribavirin |
M11-652 (Aviator) |
Abbott |
- |
2012/10/15 �t�F�[�Y2b�����ɂ������ǍD�Ȍ��� |
�v���e�A�[�[�j�Q��
�i���j |
BI 201335 NA
�i1��1��o���j |
�x�[�����K�[�C���Q���n�C�� |
- |
2011/04/06 �t�F�[�Y2�����ɂ������ǍD�Ȍ��� |
�v���e�A�[�[�j�Q��
�i����j |
TMC435 |
Medivir AB |
- |
2011/05/20 �t�F�[�Y2�������{�� |
�k�N���I�`�h�|�������[�[�j�Q��
�@Sofosbuvir |
GS-7977
(�o����) |
Gilead Science |
- |
2013/02/04 �t�F�[�Y3�����ŗǍD�Ȍ��� |
| �|�������[�[�j�Q�� |
GS 9190 |
Gilead Science |
- |
�o�Q���{�� |
�|�������[�[�j�Q��
�@�t�B���u�r�� |
�@ |
�t�@�C�U�[ |
- |
�@ |
| �|�������[�[�j�Q�� |
R1626 |
���V�� |
- |
�@ |
| �|�������[�[�j�Q�� |
JTK-853
(�o����) |
���{�����Y�� |
- |
�C�O�o�P���{�� |
| �k�N���I�`�h�̃|�������[�[ (NS5B) �}���� |
BMS-986094 |
Bristol-Myers Squibb |
- |
2012/08/23 �J�����~ |
| �̍d�ρE�̊��ւ̐i�s�j�~ |
ME3738
(�o����) |
Meiji Seika�t�@���} |
- |
2012/04/18 �J�����~ |
|
|
���P �v���e�A�[�[�j�Q�܁F�E�C���X�^���p�N�������ߒ���j�Q�����B�b�^�̉����Â̎������Ɉʒu�t������B�����Ö@�ɏ�悹���邱�ƂŎ��������ő�Q�{�߂��Ɍ��シ��D�ꂽ�R�E�C���X��p���m�F����Ă���B
���Q �|�������[�[�j�Q�܁F�E�C���X��`�q��������̂�j�Q�����B |
|
�@ |
| �i�����ǁj |
|
|
|
�@���A�����G�C�Y�v��i�t�m�`�h�c�r�j��2011�N6��3���A���E�̃G�C�Y�����ґ�������N�����_�Ő��v�R�S�O�O���l�ȏゾ�����Ɣ��\�����B�V�K�������͔N�X�����Ă��邪�A�ߋ��P�O�N�ԂŊ����҂��V�O�O���l���������B
�@�t�m�`�h�c�r�͂Q�O�P�T�N�܂łɁA���Ȃ��Ƃ��N�ԂQ�Q�O���h���i��P���V�W�O�O���~�j�̋��o��v���B���Ꮚ�����ւ̎��Öy�ɂ��A�Q�O�N�܂łɂP�Q�O�O���l�̐V���Ȋ�����h�������Ƃ��Ă���B
|
|
| ��ʖ� |
�u�����h�� |
�̔���� |
���l |
HIV�C���e�O���[�[�j�Q��
�@�����e�O���r�� |
�A�C�Z���g���X
Isentress
�i1��2�^�j |
Merck & Co., Inc./MSD |
2008/07/07 �����Ŕ���
���E���̃C���e�O���[�[�j�Q��
2007�N����s�B���E�W�T�J���ȏ�ŏ��F
2012�N ���E���� 1,515�S��$ |
HIV�C���e�O���[�[�j�Q��
�@�h���e�O���r�� |
S-349572
Tivicay
�i�P���P�^�A
�u�[�X�g�܂Ȃ��j |
VIIV |
2013/12/05 �������F�\��
2013/11/26 ���B��CHMP���珳�F��������
2013/08/15 �č��ɂ����鏳�F���� |
HIV�C���e�O���[�[�j�Q��
�@Elvitegravir�F�G���r�e�O���r�� |
JTK-303 |
���{�����Y��
�M���A�h�E�T�C�G���V�Y |
�J����
�č��M���A�h�E�T�C�G���V�Y�Ђ֓��{�������S���E�̊J���E���Ɖ����o
���{�����Y�ƋN�� |
�z����
�@�G���r�e�O���r��
�@�R�r�V�X�^�b�g
�@�G���g���V�^�r��
�@�e�m�z�r�� �W�\�v���L�V���t�}���_�� |
�X�^���r���h�z���� |
���{�����Y��
�M���A�h�E�T�C�G���V�Y |
2013/05/27 ���B���F
2013/03/25 �������F
2012/08/27 ����F
|
| �v���e�A�[�[�j�Q�� |
�@ |
�@ |
�@ |
�@cobicistat�F�R�r�V�X�^�b�g
�@�i�v���e�A�[�[�j�Q�ܑ�����j |
�@ |
���{�����Y��
�M���A�h�E�T�C�G���V�Y |
2012/06/28 ��\�� |
�@atazanavir sulfate
�@�A�^�U�i�r�����_�� |
Reyataz
���C�A�^�b�c |
Bristol-Myers Squibb |
2012�N ���E���� 1,521�S��$
2003/12 ���F |
| �@�_���i�r���Fdarunavir |
PREZISTA
�v���W�X�^�i�C�[�u |
�����Z���t�@�[�} |
2011�N ���E���� 1,211�S��$
2012/07/13 800�r���܌^�lj� �����\��
2006�N6���@�č��ŏ��F
2007�N2���@���B�ŏ��F
2007�N11�� ���{�ŏ��F |
�@���g�i�r���Fritonavir
�@�i�v���e�A�[�[�j�Q�ܑ�����j |
�m�[�r�A |
�A�{�b�g �W���p�� |
1999/08 ���F |
| �@�C���W�i�r�� |
�N���L�V�o�� |
MSD |
1997/03 ���F |
| �@���V���_�T�L�i�r�� |
�C���r���[�[ |
���O���� |
1997/09 ���F |
| �@�T�L�i�r�� |
�t�H�[�g�x�C�X |
���O���� |
2000/04 ���F |
| �@�l���t�B�i�r�� |
�r���Z�v�g |
���{�����Y�� |
1998/03 ���F |
| �@�A���v���i�r�� |
�v���[�[ |
�@ |
1999/09 ���F |
| �@���s�i�r���E ���g�i�r�� |
�J���g�� |
�A�{�b�g �W���p�� |
2000/12 ���F |
| �@�z�X�A���v���i�r�� |
���N�V���@ |
VIIV |
2005/01 ���F |
�i�j�_�n�j�t�]�ʍy�f�j�Q��
NRTI=Nucleoside Reverse Transcriptase Inhibitor |
�@ |
�@ |
�@ |
| �@�W�h�u�W���E���~�W�� |
�R���r�r��
Combivir |
VIIV |
1999/06 ���F
2011�N�̔����F5���h�� |
| �@���~�u�W���E���_�A�o�J�r������ |
�G�v�W�R��
Epzicom |
VIIV |
2005/01 ���F
2011�N�̔����F10���h�� |
| �@�W�h�u�W�� |
���g���r�� |
VIIV |
1987/09 ���F |
| �@�W�_�m�V�� |
���@�C�f�b�N�X |
�u���X�g���E�}�C���[�Y |
1992/06 ���F |
| �@�U���V�^�r�� |
�n�C�r�b�g |
���O���� |
1996/04 ���F |
| �@���~�u�W�� |
�G�s�r��
Epivir |
�O���N�\�E�X�~�X�N���C�� |
1997/02 ���F |
| �@�T�j���u�W�� |
�[���b�g |
�u���X�g���E�}�C���[�Y �X�N�C�u |
1997/07 ���F |
| �@�A�o�J�r�� |
�U�C�A�W�F�� |
VIIV |
1999/09 ���F |
| �@*�e�m�z�r�� |
�r���A�[�h |
�M���A�h�E�T�C�G���V�Y/���{�����Y�� |
2004/04 ���F |
| �@*�G���g���V�^�r�� |
�G���g���o |
�M���A�h�E�T�C�G���V�Y/���{�����Y�� |
2005 ���F |
�i��j�_�n�j�t�]�ʍy�f�j�Q��
NNRTI=Non-Nucleoside Reverse
Transcriptase
Inhibitor |
�G�W�������gTM��25mg |
�����Z���t�@�[�}
Johnson & Johnson |
2012/02/07 �����\��
2010/05/20 FDA���F
Tibotec Pharmaceuticals�N���@ |
| �@�����s�r���� |
�@ |
�@ |
�@ |
| �@�l�r���s�� |
�r���~���[�� |
���{�x�|�����K�|�C���Q���n�C�� |
1998/11 ���F |
| �@*�G�t�@�r�����c |
�X�g�b�N����
Sustiva |
MSD |
1999/09 ���F |
| �@�f���r���W�� |
���X�N���v�^�[ |
�t�@�C�U�[ |
2000/02 ���F |
| �@�G�g���r���� |
�C���e�����X |
�����Z���t�@�[�} |
2009/01/19 ���{�Ŕ���
Tibotec Pharmaceuticals�N�� |
����
�@�i�G�t�@�r�����c/�e�m�z�r��/�G���g���V�^�r���̔z���܁j |
�A�g���v��
Atripla |
�M���A�h�E�T�C�G���V�Y |
2011�N ���E���� 3,200�S��$
�i�M���A�h�E�T�C�G���V�Y : 863�S��$�j |
�@�j�_�n�t�]�ʍy�f�j�Q��
�@�i�e�m�z�r��/�W�\�v���L�V���̔z�����j |
�c���o�_
Truvada |
�M���A�h�E�T�C�G���V�Y |
�@ |
| �@�i�e�m�z�r��/�G���g���V�^�r���̔z�����j |
�c���o�_
Truvada Combination Tablets |
�M���A�h�E�T�C�G���V�Y/���{�����Y�� |
2012/07/16 ���̗\�h��Ƃ��ĕč��ŏ��F
2005 ���F |
|
|
���C���e�O���[�[�j�Q��
�@�C���e�O���[�[�j�Q���͐V�����N���X�̍RHIV��ł���A�E�C���XDNA���q�gT�P�����p���̐��F��DNA�ɑg�ݍ��܂��̂�j�Q���邱�Ƃɂ��AHIV����������̂�h���܂��B���̃C���e�O���[�V�����̉ߒ��́AHIV�̕����ɕs���ł��B�C���e�O���[�[�j�Q���͂��̃��j�[�N�ȑj�Q�@����HIV�̖�ܑϐ����ɑΏ����ĐV�������Ö@���m�����邽�߂ɑ傫�Ȃ�������������Ă����A�����A�C���e�O���[�[�j�Q���͍ł������̋����RHIV���1�Ƃ��āA�܂�����p�̏��Ȃ���܂Ƃ��ĔF�߂��Ă��܂��B
���v���e�A�[�[�j�Q��
�@�����זE�̒���HIV�̕��i������鎞�AHIV�`��(gag-pol)���o��"�͂���"�̖�����HIV�v���e�A�[�[�B�͂��݂̐n�ɂ͂܂荞��œ������ז��������A���nHIV���ł��Ȃ��B�v���e�A�[�[�j�Q�܂͐��n������������HIV���ł���̂�H���~�߂邱�ƂɂȂ�B
���i��j�_�n�j�t�]�ʍy�f�j�Q��
�@�j�_�Ɏ����\���������Ȃ��t�]�ʍy�f�j�Q�܂̂��ƁB�t�]�ʍy�f�Ɍ������A�������ʂ̗��̍\����ς��邱�Ƃɂ��y�f�̑j�Q���ʂ����܂��B�i��j�_�n�j�t�]�ʍy�f�j�Q�܂͒P�܂ł����ɋ��͂�HIV�̑��B��}�����܂��B�������킸��1�����̈�`�q�ψقőϐ��ƂȂ�A�������Z���Ԃɂ�����B�]���ĕ��p�Ö@����{�ł��B |
|
�@ |
|
|
|
�@�s���ǂ́A�����ɑ���ߏ�ȑS�g�����ǔ������������d�Ăȕa�Ԃł��B�d�Ǘ�ł́A�s���ǐ��V���b�N�⌌�Ǔ��Ìŏnj�Q�A����s�S�������N�������߁A���S�������ɍ����Ȃ�܂��B���݁A�d�ǔs���ǂ̎��Â͑I�����������Ă���A�č��ł͖��N20���l�ȏオ�d�ǔs���ǂŖ��𗎂Ƃ��Ă���ƌ����Ă��܂��B |
|
|
|
�@
���s���ǂ̎��� |
|
�@ |
|
|
|
�R�������Ƃ́A���������Y�����A�ق��̔������̑��B��}�����镨���̑��́B�R���������܂ލR�ۍ܂́A�ۂ����B����̂ɕK�v�ȑ�ӌo�H�ɍ�p���邱�Ƃōۂɂ̂ݑI��I�ɓŐ��������i�l�̂ւ̓Ő��͂���ɔ�ׂ͂邩�ɏ������j���w�����ł��B
���E�ōŏ��ɍR���������������ꂽ�̂�1929�N�̂��Ƃł��BA.Fleming�ɂ���ĐJ�r����P�����ꂽPenicillin���ŏ��ł��B���̔������_�@�Ƃ��Ă��܂��܂ȍR���������T���E���������Ɏ���܂����B
�R�������������Ƃ��З͂�����̂͊����ǂɑ��Ăł��B�̂͌��݂قLj�w�����B���Ă��炸�A�ԗ��E���j�E�R�����Ȃǂɑ�\����銴���ǂ͋��ЂƂ���Ă��܂����B�D�ꂽ�R�������������E�J���ɂ��A�����ł͊����ǂŎ��S����l�͂��Ȃ菭�Ȃ��Ȃ��Ă��܂��B
�ŋ߂ł͉Ȋw�̐i���ɂ���āA������������ɍR�ۗ͂���������܂��������邱�Ƃ��\�ƂȂ�A���������������ł͍R�������̒�`����O��邽�߂ɁA�u�R�ۍ܁v�Ƃ����Ăѕ������邱�Ƃ�����܂��B����Ɍ����Ɍ����R���������R�ۍ܂Ɋ܂܂�邱�ƂɂȂ�A��������܂Ƃ߂Ɂu�R�ۍ܁v�ƌĂԂ��Ƃ��������̂ł��B
���ׂɔ����C�ǎx���Ȃǂ�}����o���^�̍R�ۍ܂͍�p���J�j�Y���ɂ���ăZ�t�F���n�A�j���[�L�m�����n�A�}�N�����C�h�n���唼���߂܂��B�Z�t�F���n�͉���`����́u�t�����b�N�X�v���A�j���[�L�m�����n�͑��O���́u�N���r�b�g�v�����|�I�ȃV�F�A�������Ă��܂��B�}�N�����C�h�n�͑吳�x�R���i�́u�N�����X�v����\�I�Ȑ��i�ł��B
�����̍R�ۖ�s��͂T,�O�O�O���~��i�㔭���j�ƌ����Ă��܂����A���N�����̃y�[�X�ŏk�����Ă��܂��B |
|
| ��ʖ� |
�u�����h�� |
�̔���� |
�������� |
���l |
| �Z�t�F���n |
�����R�ۍ�/�Z�t�F��
�@�Z�t�J�y�� �s�{�L�V�� |
�t�����b�N�X |
����`���� |
219���~
�i2011/3�j |
�O�����z���ۂ̂ق��A�咰�ۂ�C���t���G���U�ۂȂǃO�����A���ۂɋ����R�ۗ͂����܂��B�@ |
| �L�m�����n |
�����R�ۍ�/�j���[�L�m����
�@���{�t���L�T�V�� |
�N���r�b�g |
���O��
J & J�A�T�m�t�B�E�A�x���e�B�X |
324���~
�i2011/3�j |
2011/03 ���E���� 691���~
�畆�����ǁA�ċz�튴���ǁA��A�튴���ǁA�w�l�Ȋ����ǁA��Ȋ����ǁA���@�Ȋ����ǁA���Ȋ����ǂȂǍL���͈͂̊����ǂ̎��ÂɎg�p����܂��B |
�j���[�L�m�����n�R�ې���
�@�p�Y�t���L�T�V�����V���_�����ˉt |
�p�V��
�p�Y�N���X |
�吳�x�R���i
�c�ӎO�H���� |
- |
2010/07/23 ���\�E���ʒlj����F�擾
�K���ێ�F�u�x�����ہv�̒lj�
�K���ǁF�u�s���ǁv�̒lj��@ |
�o�������R�ۍ�
�@���V���_�K���m�L�T�V�����a�� |
�W�F�j�i�b�N
(�o����) |
�吳�x�R���i/
�A�X�e���X���� |
45���~
�i2011/3�j |
2007/07/31�������F
���\�E���ʁF�����E�A�����A�G�����i�G�����͉��A�G�����͔^ᇂ��܂ށj�A�}���C�ǎx���A�x���A�����ċz��a�ς̓����A�������A���@�o�� |
| �}�N�����C�h�n |
�����R�ۍ�
�@�N�����X���}�C�V�� |
�N�����X |
�吳�x�R���i |
229���~
�i2011/3�j |
��Ƀu�h�E����,�����T����,�C���t���G���U��,�܂��}�C�R�v���Y�},�N���~�W�A�ȂǂɌ��͂������̂ŁA�畆,�ċz��E��A��E���@�E���ȗ̈�Ȃǂ̊����ǂɍL���p�����܂��B�@ |
| �@�\���X���}�C�V�� |
CEM-101 |
Cempra, Inc.
�x�R���w�H�� |
- |
2013/09/06�@FDA���p�h�c�o�w��
2013/05/14�@�x�R���w�A���C�Z���X�_������
�x�����ہA�}�C�R�v���Y�}�ɑ������R�ۊ����������Ƌ��ɁA��r�I�����Ɖu������p�i�R���Ǎ�p�j��L���� |
| ���̑� |
�����R�ۍ�/�J���o�y�l���n
�@�����y�l�� |
�����y�� |
����{�Z�F���� |
122���~
�i2012/3�j |
1995�N6���@�������F
�O�����z���ہE�O�����A���ۂɂ�钆���x�ȏ�̊e�튴���ǂɕ��L���g�p����Ă��܂��B |
��-���N�^�}�[�[�j�Q�ܔz���R����������
�@���˗p�^�]�o�N�^���i�g���E���E�s�y���V�����i�g���E�� |
�]�V�� |
�吳�x�R���i
��Q��i�H�� |
148���~
�i2011/3�j |
2008/07/16�������F
���\�E���ʁF�s���ǁA�x���A�t᱐t���A���G���N���� |
�V�K�������O���R�y�v�`�h�n
�@�e���o���V�� |
���B�o�e�B�u |
�A�X�e���X���� |
- |
2010/05/23�@EU���F���� |
|
|
�@ |
|
|
|
�@�ԕ��ǂ�1960�N�ォ�瑝���n�߁A���݂ł͓��{�l�̖�Q���A�A��2400���l���ԕ��NJ��҂ł���ƌ����Ă��܂��B�����ƂȂ�ԕ��͓��{�ł̓X�M��q�m�L�������̂ł����A�C�l�Ȃ�L�N�ȂȂǂT�O��ȏ�̐A���ɂ��ԕ��ǂ��m�F����Ă��܂��B
�@�X�M�ɂ��ԕ��ǂ����{�ŋ}�����Ă��錴���Ƃ��ẮA����E����ɖ؍ޗp�Ƃ��ēs�s�ߍx�ɐA����ꂽ�X�M���A�����C�O����̖؍ނ��g����悤�ɂȂ������ƂȂǂŐ��Ȃ��܂ܑ�ʂɎc��A���傤�NJJ�Ԏ������}���Ă��邱�Ƃ�A�����ԂȂǂ̔r�K�X�Ɋ܂܂��ׂ��������ԕ��ƌ��т��A�Ǐ�������N�������Ȃǂ��w�E����Ă��܂��B
�@�ԕ��ǂ̈�Ô��2000���~�A��Ô�ȊO�́A�s�̖��A�}�X�N�A�[���Ȃǂ�����ԕ��ǎs���1000���Ƃ������Ă��܂��B�ԕ��nj�����i�̎s��͐����������߁A�����Ƃ͐V��̊J���̐����������Ă��܂��B |
|
�@ |
|
�C�O�̎��� |
|
�@�l���̂P�����̂S�O�O�O���l���ԕ��ǂƂ����č��ł́A�ӏt���珉�Ăɂ����Ă̓��M��C�l�Ȃ̐A���A�Ă���H���ɂ����Ă͓��[�̃u�^�N�T���ԕ������܂��B�ԕ��V�[�Y���͒g�~�Ɩҏ��ɂ���ď��X�ɒʔN��������܂��B
�@���ł͂ł͐l���̖�Q�����ԕ��ǂȂǂɋꂵ��ł��邻���ł��B���B�����ł̓C�l�Ȃ̐A�������S�B�n���m�L�A�|�v���A�X�M��n���m�L�A�J�o�m�L�Ȃǂ��ԕ������܂��B�X�y�C����C�^���A���ԕ��ʂ������A�Z���r�A�Ȃǒ��������܂߁A���B�S�悪�ԕ��̉e��������܂��B
�@�P�X���I�����̉p���ŁA�������������_�Ƃ̐l�X���Ǐ��i�����̂��ԕ��ǂ̍ŌÂ̗�̈�Ƃ���A���Ăł͍��ł��ԕ��ǂ��u�͂ꑐ�M�v�ihay fever�j�ƌĂԂ����ł��B |
|
�@ |
|
�ԕ��ǂ̃��J�j�Y�� |
|
�@�ԕ����̂ɓ���ƁA�̓��̖Ɖu�����ʼnԕ��Ɋ܂܂�鐬�����ٕ��i�R���j�ƔF�����Ăh�f�d�R�̂Ƃ�������ȃ^���p�N�����ł��܂��B���̍R�̂����܂�ƁA�Ăё̓��ɓ����Ă����ԕ��Ƃ������A���ǂ������N�����q�X�^�~���Ȃǂ̕�������o���܂��B���ꂪ�ڂ�@�̔S���ɍ�p���A������݂�@���A�ڂ̂���݂Ȃǂ������N�����܂��B |
|
�@ |
|
�R�q�X�^�~���� |
|
�@�a�@�ōŋߏ��������R�q�X�^�~���܂͑�Q����ƌĂ�A�s�̖�ɔz������鋌����̂��̂�肸���Ɩ����Ȃ�ɂ����Ȃ��Ă��܂��B���ł����ړx�������̂́A�Q�O�O�S�N�H�ɔ������ꂽ�V�F�����O�E�v���E�Ђ́u�N�����`�����f�B�^�u���v�ł��B��ʓI�ɍR�q�X�^�~���܂̕��p��͎����Ԃ̉^�]�������ׂ��Ƃ���Ă��܂����A���̖�̓T�m�t�B�E�A�x���e�B�X�Ђ́u�A���O���v�ƂƂ��ɁA�Y�t�����ł����ɒ��ӊ��N�͂���Ă��܂���B���Ȃ��ň��߂�֗�����A������̕��p�ōςނ��Ƃ��Ă��܂��B
�@�A���O���i�T�m�t�B�E�A�x���e�B�X�j�@�@�Q�O�O�O�N�P�P�������A�����V�F�A�g�b�v�B����ł������Ȃ�ɂ����B
�@�N�����`�����f�B�^�u���i�V�F�����O�E�v���E�j�@�@�Q�O�O�S�N�P�P�������@�@���Ȃ��ň��߂�B���ɓ����ƂP�b�ŗn����B
�@�@�@�@�@�@�@�@�@�@�@�@�@�@�@�@�@�@�@�@�@�@�@�@�@�@�@�@�A���O�����l�A�����Ȃ�ɂ����B |
|
�@ |
|
�����Ö@ |
|
�@������Ái���j�@�́A�ԕ��̃G�L�X�𒍎˂��ăA�����M�[��������߂�Ɖu�Ö@�̈��ŁA���ݗB��̍����Ö@�ł��B�L�����͂V�`�W���ƍ����̂ł����Q�`�R�N�ȏ㑱����K�v������A�����܂�ɋN����d�Ăȕ���p������A�������t�������Ƃ����Ă��܂��B����ɑ��u�㉺�v�Ö@�͒��˂�葽���̃G�L�X�𓊗^�ł��A���Â���߂Ă��R�N�Ԃ͌��ʂ������܂��B�d������p�����Ȃ��A���҂̕��S���������̂ŏ����ɂ��g���₷���Ƃ����Ă��܂��B |
|
�@ |
|
| ��ʖ� |
�u�����h�� |
�̔���� |
�������� |
���l |
| �t�F�L�\�t�F�i�W�����_���ɉ��_�v�\�C�h�G�t�F�h������z�������o���z���� |
�f�B���O���z����
�i�o���z���܁j |
�T�m�t�B |
- |
2012/12/25 �������F |
��2����R�q�X�^�~����
�@�t�F�L�\�t�F�i�W�����_�� |
�A���O�� |
�T�m�t�B |
629���~
�i2011/12�j |
2000�N �������� |
| �����^�W�� |
�N�����`�� |
Merck & Co., Inc./
����`���� |
100���~
�i2011/3�j |
2002�N �������� |
��2����R�q�X�^�~����
�@���_�Z�`���W�� |
�W���e�b�N |
UCB/�O���N�\�E�X�~�X�N���C��/���O�� |
96���~
�i2010/3�j |
1998�N ��������
���E���� 82�S��$�i2010�N�j |
��2����R�q�X�^�~����
�@���_�I���p�^�W�� |
�A�����b�N |
���a���y�L���� |
291���~
�i2011/12�j |
2001�N3�� ��������
�I��I�q�X�^�~��H1��e�̝h�R��p�����p�Ƃ��� |
| �v�������J�X�g���a���J�v�Z�� |
�I�m���J�v�Z�� |
�����i�H�� |
251���~
�i2011/3�j |
�@ |
| �x�|�^�X�`���x�V���_�� |
�^���I���� |
�c�ӎO�H���� |
- |
�W�F�l���b�N���@ |
�㉺�Ɖu�i������j�Ö@��
�@�A�����Q���G�L�X |
�V�_�g�����X�M�ԕ��㉺�t |
������i������� |
- |
2014/01/17 �������F
2012/09/14 ������III���Տ������̑���
2010/03/11 �X�M�ԕ��G�L�X�̐㉺���^�ɂ�錸���쎡�Ö�̊J�������̊J�n |
|
|
�@ |
|
�A�����M�[���@������ |
|
| ��ʖ� |
�u�����h�� |
�̔���� |
�������� |
���l |
| �f�L�T���^�]���V�y�V���_�G�X�e�� |
�G���U�X |
���{�V�� |
- |
�@ |
| ���}�g���o�� |
�o�C�i�X |
���{�V�� |
|
�@ |
| ���_���{�J�o�X�`�� |
���{�X�`�� |
�W�F�l���b�N�� |
|
�@ |
| �v���X�^�O�����W��D2��e�̝h�R�� |
S-555739 |
����`���� |
- |
2012/06/14 ����Տ���2���������� |
|
|
�@ |
|
|
|
�@���݁A���{�S���Ŋ߃��E�}�`�ɔY�ފ��҂�100���l�Ƃ������A���̐��͍���ɂƂ��Ȃ��N�X��������X���ɂ���܂��B�j���̊�����1��4�ƈ��|�I�ɏ����ɑ����A���ǔN���30�`50�Α�A�Ƃ���40�Αオ�����Ƃ��������Ƃ��킩���Ă��܂��B���̌����ɂ́A�����̈�`���q�Ƌi���Ȃǂ̊����q���֗^���Ă��邱�Ƃ����炩�ƂȂ��Ă��܂��B |
|
�@ |
|
�����w�I���� |
|
�@�߃��E�}�`���ẤA�����w�I���܂̓o��Ŋ�����ڕW�Ƃ��邱�Ƃ��\�ɂȂ�A�傫���i�����܂����B�s��ɐ�߂鐶���w�I���܂̊������N�X���܂��Ă���A2008�N�ɂ�68%�ƂȂ�܂����B |
|
| ��ʖ� |
�u�����h�� |
�̔���� |
�������� |
���l |
| �G�l�^���Z�v�g |
�G���u����
Enbrel |
�A���W�F��/�t�@�C�U�[/���c��i�H�� |
414���~
�i2012/3�j |
2012�N ���E���� 7,973�S��$
1998�N�ɕč��ɂ����Đ��E�ŏ��߂ĔF���ꂽ�����w�I���� |
�R�q�gTNF-?���m�N���[�i���R��
�@�C���t���L�V�}�u |
���~�P�[�h
�i�Ö����ˁj |
�Z���g�R�A/Merck & Co., Inc./�c�ӎO�H���� |
663���~
�i2012/3�j |
2010�N ���E���� 7,324�S��$ |
�q�g�^�R�q�gTNF�����m�N���[�i���R�̐���
�@�S�����}�u |
�V���|�j�[R�牺��50mg�V�����W
�i�牺���ˁE�����j |
�Z���g�R�A/�����Z���t�@�[�}/�c�ӎO�H���� |
9���~
�i2012/3�j |
2011/09/15 ���{�Ŕ���
2009/04 �č��A�J�i�_�ŏ��F�擾
2006/08/21 �c��&�ݾ� �����J���E�����̔� |
�q�g�^�R�q�g�s�m�e���m�N���[�i���R��
�@�A�_�����o�u |
�q���~��
HUMIRA |
�A�{�b�g/�G�[�U�C |
133���~
�i2011/3�j |
2012�N ���E���� 9,265�S��$
2008/04/16 �����ŏ��F�擾�i�G�[�U�C�j |
�q�g���R�q�gIL-6 ���Z�v�^�[���m�N���[�i���R��
�@�g�V���Y�}�u |
�A�N�e�~�� |
���O����/���V�� |
171���~
�i2012/12�j |
2008/04/16�@�����ŏ��F�擾
2009/01/21�@���B�ŏ��F�擾
2010/01/09�@�č��ŏ��F�擾
���{�őn��ꂽ���߂Ă̍R�̈��i |
T�זE�I��I���h�����ߍ�
�i���S�q�g�^�RPD-1�R�́j
�@�A�o�^�Z�v�g |
�I�����V�AR IV |
�u���X�g���E�}�C���[�Y �X�N�C�u�^�����i |
�| |
2013/08/27 �牺��125mg �V�����W1mL�v�V����
2011/09/21 �����i�ƒ�g
2010/09/21 ��������
�č��ł�2005�N12���ɏ��F
���B�ł�2007�N5���ɏ��F
2010�N ���E���� 733�S��$ |
�RTNF-���R��
�@�Z���g���Y�}�u�y�S�� |
�V���W�A |
UCB/�A�X�e���X���� |
�| |
2012/12/25 �������F
2009/07/08�@���B�ŏ��F�擾
2009/05/25�@�č��ŏ��F�擾
�u�B���PEG������TNF�R�́i�牺�����܁j�v�i���^�Ԋu�̓t�F�[�Y�Q�A�R�����ł͂Q�T�ԂɂP�^�j |
�RIL-6���m�N���[�i���R��
�@Sirukumab�i�V���N�}�u�j |
CNTO 136 |
Johnson & Johnson/GSK |
�| |
2012/08/23 P3�����J�n |
| ���S�q�g�RIL17A���m�N���[�i���R�� |
AIN457 |
�m�o���e�B�X |
�| |
2011/10/28 ��II���Տ��������ʂ\
P3���{�� |
�RBAFF���m�N���[�i���R��
Tabalumab |
�@ |
Eli Lilly and Company |
�| |
2013/02/07 �J���f�O |
�RCD20���m�N���[�i���R��
�@�I�N�����Y�}�u�iocrelizumab�j |
�@ |
�W�F�l���e�b�N/���V��/�o�C�I�W�F���E�A�C�f�b�N |
�| |
2010/05/19 �J�����~ |
|
|
�@ |
|
�Ɖu�}���E������Ȃ� |
|
�@�����w�I���܈ȊO�̍R���E�}�`�܂ł́A�߃��E�}�`���Â̑��I���Ƃ��Đ�������Ă���Ɖu�}���܂̃��g�g���L�T�[�g���A�����w�I���܂Ƃ̕��p�Ö@�ɂ����т�L���Ă��܂��B |
|
| ��ʖ� |
�u�����h�� |
�̔���� |
�������� |
���l |
�t�_��ӝh�R��
�@���g�g���L�T�[�g |
���E�}�g���b�N�X
���g�g���L�T�[�g |
�t�@�C�U�[
���ق� |
�| |
���{�ɂ�������I��� |
�����C�����R���E�}�`��FDMARD
�@�T���]�X�t�@�s���W�� |
�A�U���t�B�W�� |
�t�@�C�U�[/�Q�V���� |
41���~
�i2011/3�j |
1995�N���� |
�����C�����R���E�}�`��FDMARD
�@�u�V���~�� |
���}�`�� |
�Q�V���� |
39���~
�i2011/3�j |
���Бn���i�A1987�N���� |
�����C�����R���E�}�`��FDMARD
�@�C�O���`���h |
�P�A����
�R���x�b�g |
�G�[�U�C/�x�R���w�H�� |
�| |
2012/09/12 ��������
2011/08/31 �����\�� |
�~�]���r��
�i�Ɖu�}����j |
�u���f�B�j�� |
�������t�@�[�} |
65���~
�i2011/3�j |
�@ |
|
|
�������C�����R���E�}�`��iDMARD�j
�@DMARD�iDisease Modifying Anti-Rheumatic
Drug�j �́A�a�C�̖{�Ԃ��R���g���[������Ƃ����Ӗ��Ŏ����C�����R���E�}�`��ƌĂ�Ă��܂��B�߃��E�}�`�ɂ����ĉ��ǂ��N���������ƍl�����Ă���Ɖu�ُ�Ȃǂ��R���g���[�����邱�Ƃ����҂���܂��B
�@�@ |
|
�V�����@����L����ᕪ�q�ʍR���E�}�`�� |
|
�@�߃��E�}�`�̎��Â͐������܂̓����Ŏ��Ð��т����サ�܂������A�Տ��I�������͂R���ɉ߂��܂���B�������܂͍����ŁA�_�H�����˂݂̂̂��߁A���Ó�����p��������Ȋ��҂����Ȃ��Ȃ��Ȃljۑ肪�w�E����Ă��܂��B�o���R���E�}�`��őS���V�����N���X�̋@����L����i�`�j�R�j�Q��́A��\�I�ȃT�C�g�J�C���̏��`�B���q�i�����i�����������@�������������j��W�I�Ƃ����ᕪ�q�ʍR���E�}�`��ł��B�C�O�t�F�[�Y�R�ł͂c�l�`�q�c�̎��Â������\�����ʂ������Ȃ����������x����d�x�̊������q�`���ҁi�U�P�P�l�j�ł̂R�J����̂`�b�q�Q�O�B�����́A�v���Z�{�Q�Q�U�D�V���ɑ��A�T�~���O�������^�Q�T�X�D�W���A���P�O�~���O�������^�Q���U�T�D�V���ŗL�ӂȒB�����������܂����B�Տ��I�L�����͂P�T�Ԉȓ��ɔ������A�����ōł��ėp����Ă���s�m�e�j�Q��ɕC�G����v���Ȍ��ʂ��m�F����Ă��܂��B |
|
| ��ʖ� |
�u�����h�� |
�̔���� |
�������� |
���l |
JAK�iJanus Kinase�j�j�Q��
�i�߃��E�}�`�̕W�I�Ɖu���ߖ�ю����C����j
�@�g�t�@�V�`�j�u �N�G���_�� |
XELJANZ
�[�������c
(�o����) |
�t�@�C�U�[/���c��i�H�� |
�| |
2013/03/25 �������F
2012/11/06 ����F
���{�ł͊߃��E�}�`��ΏۂƂ��ėՏ���3�����������{���B�C�O�ł́A��ᝁA�N���[���a����ђ�ᇐ��咰���ł��J����i�߂Ă��� |
| JAK�iJanus Kinase�j�j�Q�� |
ASP015K
(�o����) |
�A�X�e���X����/�����Z���E�o�C�I�e�b�N |
�| |
2012/10/02 �����Z���E�o�C�I�e�b�N�ЂƂ̃��C�Z���X�_�����
�߃��E�}�`���҂�ΏۂƂ������v3�̌����U���Տ�������č�/���B�A���{�Ŏ��{��
�A�X�e���X����N�� |
| �]�ʈ��qAP-1(Activator Protein-1)�j�Q |
T-5224
(�o����) |
�x�R���w�H�� |
�| |
AP-1��j�Q���邱�Ƃɂ��A���ǂ�ߔj���}����B���{���Ö�Ƃ��Ċ��ҁB
2008/02/08 ����P2�J�n |
|
|
�@ |
|
|
|
�@�]��Ґ��Ȃǂ̒����_�o�n�̐��₪�j��Ĕ��ǂ�����̂ŁA���ȖƉu�����̈�ƍl�����Ă��܂��B���͂̒ቺ�A���̂���d�Ɍ�����A�ዅ���ӂ邦��A�ڂ̒ɂ݂Ȃǂ̏Ǐ�̂ق��A�葫�����т��A�葫�ɗ͂�����Ȃ��A�召�ւ̔r������⎸�ցA�߂܂��A����ׂ�ɂ����A���̂����ݍ��݂ɂ����ȂǁA���낢��ȏꏊ�ɑ��푽�l�ȏǏ݂��܂��B
�@�Ǐ������ꂽ��C�a�a�炢������J��Ԃ��Ȃ��玟��ɐi�s���Ă����܂��B���̌����ɂ��Ă͖��炩�ɂȂ��Ă��܂��A���炩�̌����ŖƉu�����Ɉُ킪������A�]��Ґ��Ȃǂ̒����_�o�n�̐�����U������R�̂��o���邽�߂ƍl�����Ă��܂��B
�@�������d���ǂ́A���Ă̔��l�ɑ����A�k���ł͐l��10���l��50�l����100�l�ʂ̊��҂����܂��B�킪���ł͔�r�I�܂�Ȏ����ŁA10���l������1�`5�l���x�Ƃ���Ă��܂��B��N���l�ɔ��a���邱�Ƃ��ł������A���ϔ��a�N���30�ΑO��B�j�����1�F2�`3�ʂł��B���Ґ��̎����́A�k�Ăł͖�40���l�A���E���ł�100���l����Ɛ��肳��Ă��܂��B |
|
| ��ʖ� |
�u�����h�� |
�̔���� |
�������� |
���l |
| Interferon��1a |
Avonex
�A�{�l�b�N�X
���ˍ� |
Biogen Idec |
�| |
2011/06/07 AVONEX PEN�@EU�ɂď��F
1996�N �č��ŏ��F�A����90�����ȏ�Ŏg�p
2012�N ���E���� 2,913�S��$ |
| natalizumab |
Tysabri
�^�C�T�u��
�_�H���i��1��j |
Biogen Idec
Elan Pharmaceuticals |
�| |
2004/11/23 �č��ŏ��F
2012�N ���E���� 1,135�S��$ |
| Interferon��1a |
Rebif
���ˍ� |
�����N�Z���[�m |
�| |
���E���� 1,218�S��EUR |
| interferon beta-1b |
Betaferon
�i�x�^�t�F�����j
���ˍ� |
�o�C�G����i |
�| |
���E���� 1,028�S��EUR |
�Ĕ������^�������d���ǎ��Ö�
�@Synthetic polypeptides |
Copaxone
���ˍ� |
Teva Pharmaceutical |
�| |
���E���� 1,713�S��$ |
�X�t�B���S�V��1-�����_����e�́iS1PR�j���ߍ�
�@�t�B���S�����h���_�� |
Gilenya�F�W���j�A
�C���Z���F����
(�o����) |
�m�o���e�B�X �t�@�[�}
�i�c�ӎO�H�����j |
�| |
2012�N ���E���� 1,195�S��$
2012/06/14 ��III�����ڔ�r�����̌p�����^���� ����̐V���ȃf�[�^�ɂ����Ē����L�����ƈ��S�����������
2011/09/26 �������F�i�m�o���e�B�X�A�O�䐻���Ƌ����J���j
2011/03/21 ���B���F
2011/02/02 �X�C�X�ƃI�[�X�g�����A�ŏ��F
2010/09/21 ����F
2010/09/10 ���V�A���F
�c�ӎO�H����A�O�䐻���N���i�m�o���e�B�X�t�@�[�}�֓��o�j |
�W�q�h���I���e�[�g���f�q�h���Q�i�[�[�j�Q��
�@teriflunomide:�e���t���m�~�h |
AUBAGIO
(�o����) |
Sanofi |
�| |
2013/08/30 ���B���F
2012/09/12 ����F
2010/08/30 P3�����ŗǍD�Ȍ��� |
| cladribine�F�N���h���r�� |
(�o����) |
�����N�Z���[�m |
������ |
2011/03/02 FDA�����F��ے�
2010/09/24 CHMP���ے�I����
2010/09/03 �I�[�X�g�����A���F
2010/07/28 FDA���D��R���i�ڂɎw��
2010/07/12 ���V�A���F |
Dimethyl Fumarate
�t�}���_�W���`�� |
TECFIDERA
�iBG-12�j
(�o����) |
Biogen Idec |
�| |
FDA �̐R������ 2013�N3��28��
2012/10/12 P3�����ŗǍD�Ȍ���
2012/05/09 ���Ăɂď��F�\����̒ʒm
2011/10/21 P3�����ŗǍD�Ȍ��� |
| alemtuzumab |
LEMTRADA |
Sanofi |
�| |
2013/01/28 ����F�\����� |
| �C�u�W���X�g |
MN-166 |
���f�B�V�m�o |
�| |
2010/07/08 MN-166�̍�p�@���Ɋւ���_���f��
2008/04/08 �t�F�[�Y�Q�ɂėǍD�Ȍ���
�Ǘѐ���N�� |
| �X�t�B���S�V��-1-�����_�i�r�P�o�j��e�̍쓮��p |
ONO-4641
(�o����) |
�����i�H�� |
�| |
2012/04/17 �o�Q�����i���ۋ��������j�̌���
2011/10/04 �h�C�c�����N�Ђƃ��C�Z���X�_��
���ĉ��O�ɂł̍��ۋ��������@P2
2011�N12���̊�����\��
�����̃����p���������p�߂ɂƂǂ߂邱�Ƃŕa���ւ̃����p���Z����}�� |
| imilecleucel-T |
Tcelna |
Opexa Therapeutics
Merck Serono |
�| |
2013/02/057 Merck Serono�Ƀ��C�Z���X���^
�t�F�[�Y2b���{��
�t�@�[�X�g�C���N���X�̐V�� |
| Ocrelizumab |
�@ |
Genentech/
Biogen Idec |
�| |
�t�F�[�Y�Q |
| Laquinimod |
(�o����) |
Teva/
Active Biotech |
�| |
�@ |
|
|
��FTY720�́A�~���đ��̈��ł���lasaria sinclairii�ۂ��Y������~���I�V���imyriocin�j�����[�h�������Ƃ��āA���w�C���ɂ��n�����ꂽ�������B�זE��Q�������N�����s�זE�ɒ��ڍ�p���邱�Ƃ������ŁA�����̒P�܂������͊����̖Ɖu�}���܂ƕ��p���邱�ƂŁA����ڐA�̋��┽���}���⎩�ȖƉu�����Ȃǂ̎��Ö�ɂȂ�Ɗ��҂���Ă���B
�@�@�E�~���đ�����V���܂�悤�Ƃ��Ă���i�P�j�@�Y�w���̓�����ׁA2010/06
�@�@�E�~���đ�����V���܂�悤�Ƃ��Ă���i�Q�j�@�Y�w���̓�����ׁA2010/06
�@ |
| �i�_�o�ϐ������j |
|
|
|
�@����Љ�ɓ˓������킪���ł́A��100���l���l�X���F�m�ǎ����Ɍ������Ă��܂��B���̎����ɑ���}���̉ۑ�ƂȂ��Ă��܂��B�F�m�NJ��҂̖��ɂ�����l�X���A���c�n�C�}�[�a�Ƃ���A�ˑR�Ƃ��đ����X���ɂ���܂��B
�@���̃A���c�n�C�}�[�a�̓x�[�^�i���j�Z�N���^�[�[�iBACE1�j�ƃK���}�i���j�Z���N�^�[�[�ƌĂ�2�̍y�f���A�A�~���C�h�O��̃^���p�N���iAPP)��ؒf���A�V�l�����\������A�~���C�h�x�[�^�[�y�v�`�h�iA���j�����邱�Ƃ������ƍl�����Ă��܂��B���Ö�̊J��������2�̍y�f�̑j�Q�܂��^�[�Q�b�g�ƂȂ�A���E�������킵�Ă��܂��B
�@���݁A�A���c�n�C�}�[�^�F�m�ǂ̎��Ö�Ƃ��ẮA�A�Z�`���R�����G�X�e���[�[�j�Q��Ȃǂ���s����Ă��܂��B�������A�����̎��Ö�́A�_�o�`�B�\�̑����ɂ��Ǐ���P��p�������܂����A�A���c�n�C�}�[�^�F�m�ǂ̕a�Ԃ̐i�s��}�����邱�Ƃ͓���Ƃ���Ă��܂��B
�@�@�A���c�n�C�}�[�a�@�����s�_�o�Ȋw�����������z�[���y�[�W
�@���_�_�o�����A�]�������Í܋y�я����튯�p�܂̍����s����@ 2008�N4��30���@�x�m�o��
�@�|�F�m�NJ��҂̑���ŁA�R�F�m�Ǎ܂�2016�N�̎s���1,700���~�Ɨ\���|
|
|
�@ |
|
�̔��i�����j���̃A���c�n�C�}�[�a���Ö� |
|
| ��ʖ� |
�u�����h�� |
�̔���� |
�������� |
���l |
| �h�l�y�W�� |
�A���Z�v�g* |
�G�[�U�C |
1,055���~
�i2011/3�j |
���E���� 2,094���~�i2011/3�j |
| �A�W���T���^�� |
���~�j�[�� |
�����Z���t�@�[�}/
���c��i�H�� |
27���~
�i2012/3�j |
2011/03/22 �����̔� |
| ���}���`�����_�� |
���}���[ |
Merz Pharmaceuticals/
���O�� |
�| |
2011/04/17 �����̔� |
| ���o�X�`�O�~�� |
�G�N�Z����
Exelon/Exelon Patch
���o�X�^�b�` |
�m�o���e�B�X �t�@�[�}/
�����i�H�� |
�| |
2012�N ���E���� 1,050�S��$
2011/04/22 �������F |
|
|
�@ |
|
�J�����̃A���c�n�C�}�[�a���Ö� |
|
| ��ʖ� |
�J���ԍ� |
�J����� |
�������� |
���l |
| �@���F�_�o���� |
�@ |
�@ |
�@ |
�@ |
| a7�j�R�`�����A�Z�`���R������e�̃A�S�j�X�g�i��7R���ƽāj |
EVP-6124
MT-4666 |
EnVivo/
�c�Ӑ��� |
�@ |
2014/02/03 ���ۋ�����R���������J�n
2012/10/31 Phase2b����
2012/07/18 Phase 2b���ʔ��\
����P3����
EnVivo �ЋN�� |
| ��7R���ƽ� |
ABT-126 |
AbbVie |
�@ |
�o��Ph2 |
| ��4��2R���ƽ� |
AZD-1446 |
����ȶ |
�@ |
�o��Ph2�i���f�j |
�Z���g�j��5HT6��e�̑j�Q��p
�i5-HT6R�h�R�j |
Lu AE58054 |
Lundbeck/��ː��� |
- |
P3
2013/07/17 AAIC�Ńf�[�^�\
2012/05/29 ��2���������ǍD�Ȍ��ʂ�B�� |
| ��2cAR�h�R |
ORM-12741 |
Orion |
�@ |
�o��Ph2 |
| �@���FA���W |
�@ |
�@ |
�@ |
�@ |
A���R��
solanezumab
�@�i�\���l�c�}�u�j |
LY2062430 |
�C�[���C�E�����[ |
- |
2012/08/24 P3����(��v�]�����ږ��B��)
�A���c�n�C�}�[�^�F�m�ǂɂ�����i�s�}�� |
| BACE�j�Q |
MK-8931 |
Merck & Co., Inc. |
- |
2012/07/13 AAIC���\
Ph2/3 |
| ���i�x�[�^�j�A�~���C�h�̋ÏW�E������}���郏�N�`�� |
Lu AF20513 |
Lundbeck/��ː��� |
- |
2013/12/11 P1�J�n |
gantenerumab
�K���e�l���}�u |
�@ |
���V��
���O���� |
- |
Phase 1 |
| �RA���q�g���m�N���[�i���R�� |
BIIB037 |
�G�[�U�C |
- |
�Տ���Tb ��������i�s�� |
| �V�K���m�N���[�i���R�� |
BAN2401 |
�G�[�U�C |
- |
�A���c�n�C�}�[�^�F�m�ǂ���N��������q�̈�ƍl�����Ă���A�_�o�Ő���L����n����A���ÏW�̂ɑI��I�Ɍ������Ė��ʼn��A�]�����炱����������鐢�E�ŏ��߂Ẵ��m�N���[�i���R��
�o�C�I�A�[�N�e�B�b�N�E�j���[���T�C�G���X�ЂƂ̋��������@ |
| BACE�j�Q�� |
E2609 |
�G�[�U�C |
- |
2012/07/13 AAIC���\
������o���A���c�n�C�}�[�^�F�m�ǎ��Í܂Ƃ��ĊJ��
�Տ���U�������̊J�n�Ɍ����ď������i2014/03�j |
| BACE�j�Q�� |
�@ |
����`����/
Janssen |
- |
2012/10/31 �J�����i�̓��o |
| ACC-001 |
PF-05236806 |
Janssen AI and Pfizer
Elan |
- |
Phase 2 |
| A? vaccine |
CAD-106 |
Novartis |
- |
Phase 2 |
Beta Amyloid Inhibitor
�@bapineuzumab
�@�i�o�s�l�I�Y�}�u�j |
�@ |
Janssen AI and Pfizer
Elan |
- |
2012/08/06 �J�����~
Phase 3
���̃q�g�����m�N���i�[���R�� |
| Beta Secretase(BACE) Inhibitor |
LY2886721 |
�C�[���C�E�����[ |
- |
2013/06/13 P2�������~ |
| �@���FA���̑� |
�@ |
�@ |
�@ |
�@ |
| �_�o�זE�ی���ʂƐ_�o�ˋN�L�W���i���ʂ�L���A�a�ԓ������f���ł��������Ì��ʂ����� |
T-817MA |
�x�R���w�H��
�i�x�m�t�C�����j |
- |
2014/03/17 ���s��wiPS�זE�������Ƌ����������J�n
2013/12/04 �S�čő�̃A���c�n�C�}�[�^�F�m�ǂ̌����@�ւƋ����� �Տ��������{������
2013/01/10 ����Ph1�J�n
2008/05/14 �Տ���U��������č��ŊJ�n
�F�m�ǂ̌����ł���_�o�זE����}���A�_�o�ˋN��L����p������A�A���c�n�C�}�[�^�F�m�ǂ̍��{���Ö�Ƃ��Ċ��҂���Ă��� |
| �A���c�n�C�}�[�a�ɋN������F�m�@�\��Q�̔��ǒx�� |
AD-4833/TOMM40 |
���c��i�H�� |
- |
2013/08/27 �Տ���3�������J�n
�āE��P3 |
|
|
�@�@ |
|
�@�@�@�@�@�A���c�n�C�}�[�a�̌��������ł���x�[�^�A�~���C�h�iA���j�̐����Ɣ��ǃ��J�j�Y�� |
|
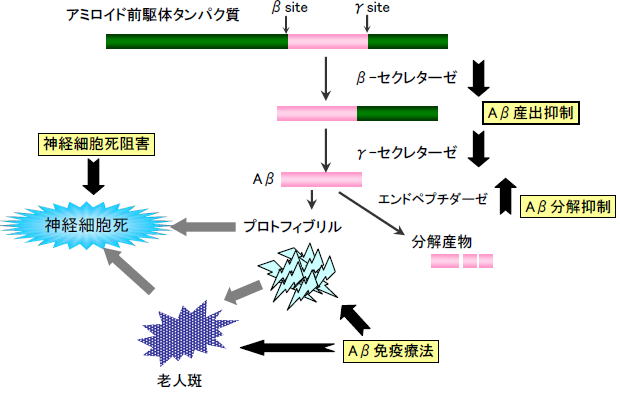 |
|
�@ |
|
|
|
�@�p�[�L���\���a�́A����҂ɂ����ăA���c�n�C�}�[�a�Ɏ�����2�Ԗڂɑ����݂��閝���_�o�ϐ������ł��B���E�I�ȗL�a���́A65�Έȏ�̖�1�`2���Ɛ��肳��Ă��܂��B
�@��ȏǏ�́A���Î��U��A�،ŏk�A�����A�p�����ˏ�Q�Ƃ������^����Q�ł��B
�p�[�L���\���a�́A�]���̐_�o�`�B�����̈��ł���u�h�p�~���v�������������ʁA�_�o�n�ɃA���o�����X�������ċN���鎾���ŁA���̎��Âɂ́A���̌��������h�p�~�����[���邽�߂̃��{�h�p(L-DOPA)���܂�p����̂��嗬�ł����A�������Âɂ��g�E�F�A�����O�E�I�t���ہh�ƌĂ�������Ԃ̒Z�k�ɂ��Ǐ�̓����ϓ���A�s���Ӊ^���Ȃǂ̉^�������ǂ������邱�Ƃ��m���Ă��܂��B |
|
| ��ʖ� |
�u�����h�� |
�̔���� |
�������� |
���l |
�p�n�I��I�h�p�~��D2��e�̍쓮��
�@�v���~�y�L�\�[�� |
�r��V�t���[�� |
�x�[�����K�[�C���Q���n�C�� |
129���~
�i2008/12�j |
2011/07/20 ���������܁i1��1�^�j��������
1997�N���F |
�h�p�~���E�A�S�j�X�g
�@�]�j�T�~�h |
�g�����[�t�@ |
����{�Z�F���� |
53���~
�i2012/3�j |
2009/3/13���� |
�h�p�~���E�A�S�j�X�g
�@�J�x���S���� |
�J�o�T�[���@ |
�t�@�C�U�[ |
25���~
�i2011/3�j |
�@ |
�h�p�~���E�A�S�j�X�g
�@�y���S���h���V���_���� |
�y���}�b�N�X |
���a���y�L����
�i���{�C�[���C�����[��菳�p�j |
21���~
�i2011/12�j |
1994�N8�� ���{�ŏ��F |
�h�p�~���E�A�S�j�X�g
�@���s�j���[�����_�� |
���L�b�v
1��1�p |
�O���N�\�E�X�~�X�N���C�� |
�| |
2012/08/28 ��������
�p�n�h�p�~����e�̍쓮�� |
�p�[�L���\���nj�Q����
�@���_�s���w�v�`�� |
�g�����[�� |
���������� |
�| |
�@ |
�p�[�L���\���a��1����
�@�A�|�����q�l���_�����a�� |
�A�|�J�C�� |
���a���y�L���� |
�| |
2012/03/30 �������F
�p�u���^�j�A�t�@�[�}�V���[�e�B�J���Y�ЋN��
�č��A�p���A�t�����X�A�h�C�c���܂�20�J���ȏ�ŏ��F |
���E���̃A�f�m�V��A2A��e�̝h�R��i�t�@�[�X�g�C���N���X�j
�@�C�X�g���f�t�B���� |
�m�E���A�X�g |
���a���y�L���� |
�| |
2013/05/29�@�����̔�
2011/06/03 �k�Ăɂ����郉�C�Z���X�_��̏I��
2010/06/03 �k�Ă̌������o�C�I�x�[���ɓ��o
2007�N4�� ��\��
�V�K��p�@����L���� |
�����ԍ�p�^COMT �j�Q��
�@Opicapone |
BIA9-1067 |
Bial
�����i�H�� |
�| |
2013/04/18�@Bial �ЂƂ̃��C�Z���X�_�����
�C�OP3�A����P1 |
�h�p�~���E�A�S�j�X�g
�@ |
���`�S�`�� |
��ː��� |
�| |
2012/01/13 �������F�\��
2011/06/08 �p�[�L���\���a�ւ̎��Ì��ʂ������Տ���III�������Ŋm�F |
|
|
L-�h�p���܁@�@�@�@�@�@�@�@�@�s�����Ă���h�p�~����₤
�h�p�~����e�̎h����@�@�h�p�~����e�̂ɒ��ڌ������A�R�p�[�L���\���a���ʂ�����
�R�R������@�@�@�@�@�@�@�@�@�h�p�~���̌����ɂ���ėD�ʂɗ������A�Z�`���R�����̓�����}������
�h�p�~�����o���i��@�@�@�h�p�~������o���Ă���_�o���h�����ăh�p�~���̕��o�𑣐i����
�m���A�h���i������[��@�]���ŕs������m���A�h���i�����̑O�앨��
MAO-B�j�Q��@�@�@�@�@�@�h�p�~���̕�����j�Q���A�h�p�~���̃h�p�~���_�o�ւ̍Ď捞��j�Q���� |
|
�@ |
|
�Q�l�ɂȂ�T�C�g |
|
|
|
�@ |
|
|
|
�@�Ă�́A���E�ی��@�ցiWHO�j�ł́u��X�̐����ɂ���ċN���閝���̔]��Q�ŁA��]�j���[�����̉ߏ蔭�˂̌��ʋN���锽��������i�Ă�j����ȏǏ�Ƃ��A����Ɏ�X�̗Տ��Ǐ�ь������������́v�ƒ�`����Ă��܂��B
�@���{�ɂ�����Ă�̗L�a����0.5�`1���ŁA�Ă҂�100���l�Ɛ��肳��Ă��܂����A���̂�����3���́A�����̖Ö@�ł̓R���g���[���ł��Ă��Ȃ��Ƃ���Ă���A�V�����@���̍R�Ă��̓o�ꂪ�w��⊳�Ғc�̂���M�]����Ă��܂��B
�@���B�ɂ����銳�Ґ��͖�340���l�Ɛ��肳��Ă��܂��B
�@2009/01/26�@�Ăǂ̌��ƂȂ�^���p�N�������̂̓�������
�@�@�@�@�@�@�@�@�@ �i�����������Ă�̔��ǃ��J�j�Y���̗����ցj
�@ |
|
| ��ʖ� |
�u�����h�� |
�̔���� |
�������� |
���l |
| �����g���M�� |
���~�N�^�[�� |
�O���N�\�E�X�~�X�N���C�� |
�| |
2008�N �������F
�p�E�G���J���Ёi��GSK�j�ɂđn��
2010�N ���E���� 504�S���� |
| �g�s���}�[�g |
�g�p�}�b�N�X/�g�s�i |
J & J
���a���y�L���� |
9���~
�i2009/3�j |
2014/01/17 �������F
2010�N ���E���� 538�S��$
1995�N �p�����F�A1996�N ����F
2007/07/31 �������F
�K���́u�ق��̍R�Ă��ŏ\���Ȍ��ʂ��F�߂��Ȃ��Ă҂̕�������
�ă}�N�j�[���E�t�@�[�}�V�[�e�B�J���Ђɂ�1979�N�ɑn�� |
| �K�o�y���`�� |
�K�o�y�� |
�t�@�C�U�[ |
�| |
2006�N �������F |
�x���]�W�A�[�s���n
�@�]�j�T�~�h |
�G�N�Z�O���� |
����{�Z�F���� |
35���~
�i2011/3�j |
1989�N �������F
���Бn�� |
| �]�l�O���� |
Elan
�����̔����G�[�U�C |
2012/07/03 �P�ܗÖ@�ɂ��ĉ��B���F
���ĂŔ̔��B�č����� 21���~�A���B���� 38���~
�����Ă��K���ǂƂ���
�i����{�Z�F����̓����i�j |
�`�l�o�`��e�̝h�R��
�@perampanel�i�y�����p�l���j |
�t�@�C�R���p
Fycompa
�i���Еi�j
(�o����) |
�G�[�U�C |
�| |
2014/01/02 �č������i12�Έȏ�̂Ă҂̕�������ɑ��镹�p�Ö@�j
2012/09/13 ���B�����i12�Έȏ�̂Ă҂̕�������ɑ��镹�p�Ö@�j
�����F��V���������{��
���Бn���̍��I��I�A���AAMPA�^�O���^�~���_��e�̝h�R��p�����t�@�[�X�g�E�C���E�N���X�̍R�Ă�� |
| ���t�B�i�}�C�h |
�C�m�x���� |
�G�[�U�C |
������ |
2007�N ���B�Ŕ̔�
���m�b�N�X�E�K�X�g�[�nj�Q�̕��p�Ö@
�i�m�o���e�B�X�Ђ���̓����i�j |
Banzel
�i�o���[���j |
2011/06/28 �J�i�_���F
2008/11/14 �č����F�i���m�b�N�X�E�K�X�g�[�nj�Q�̕��p�Ö@�j
2011/03/04 �č����F�i�o�������t�F���m�b�N�X�E�K�X�g�[�nj�Q�̕��p�Ö@�j
�i�m�o���e�B�X�Ђ���̓����i�j |
| eslicarbazepine acetate |
�[�r�j�N�X |
�G�[�U�C |
������ |
2009/4/28�@���B�ŏ��F
�iBial �Ђ���̓����i�j |
| STEDESAT |
Sepracor Inc.
�i����{�Z�F����̕č��q��Ёj |
2013/02/28 FDA ���F�ĐR����
2010/04/30 FDA �R�����ʁi���F���Ȃ��j
2009/03/31 ��\��
�iBial �Ђ���̓����i�j |
| �o���v���_�i�g���E�� |
�f�p�P��
�Z���j�J |
���a���y�L����
���a�n�� |
112���~
�i2011/12�j |
�@ |
�o���r�c�[���n
�@�t�F�m�o���r�^�[�� |
�t�F�m�o�[���A
���~�i�[�� |
���i����
������i |
�| |
�@ |
| �G�g�T�N�V�~�h |
�U�����`��
�G�s���I |
���O��
�@ |
�| |
�@ |
| ���x�`���Z�^�� |
�C�[�P�v�� |
UCB/��ː��� |
�| |
2010/09/17�@�����̔�
1999�N�@�č��ŏ��F
2000�N�@���B�ŏ��F
�u���̍R�Ă��ŏ\���Ȍ��ʂ��F�߂��Ȃ��Ă҂̕�������i���S�ʉ�������܂ށj�ɑ���R�Ă��Ƃ̕��p�Ö@�v |
| ezogabine�i�G�]�K�r���j |
Potiga |
�O���N�\�E�X�~�X�N���C��
Valeant |
�| |
2011/06/13�@FDA���F |
| �X�`���y���g�[�� |
�f�B�A�R�~�b�g |
Meiji Seika�t�@���} |
|
2012/09/28 �������F
���o�C�I�R�f�b�N�X�ЋN��
�h���x�nj�Q���� |
| ���t�B�i�~�h |
�C�m�x���� |
�G�[�U�C |
�| |
2012/08/30 �������F�F���m�b�N�X�E�K�X�g�[�nj�Q
�m�o���e�B�X�Ђ�蓱�� |
|
|
�@ |
|
|
|
�@���������ǂ͐_�o�`�B������1�ł���h�[�p�~���̓������ߏ�ɂȂ邱�Ƃɂ��A�l�X�ȏǏ�������N���������ł��B�h�[�p�~���̓����������Ȃ�ƁA���o�A�����A�ϑz�A�����Ȃǂ̏Ǐ\�ꂽ��A�_�o���ߕq�ɂȂ��ďW���͂⒍�ӗ͂��ቺ�����肵�܂��B���{�I�Ȍ����͂܂��͂�����Ɖ𖾂���Ă��܂��A��`��X�g���X�ȂǁA�l�X�Ȉ��q���ւ���Ă���ƍl�����Ă��܂��B
�@���������ǂ́A�č�������2�S������3�S���l�A���E���ł�2��4�S���l�ȏオ�늳���Ă��܂��B���������ǂ́A�j���̋�ʂȂ����l�ɔ��ǂ��A���E�I�ɂ��̗��ɐl�퍷�͂���܂���B���{�ł͖�76���l�̓��������NJ��҂����Â��Ă���A��Ë@�ւ���f���Ă��Ȃ��l��������ƁA���������ǂ̊��҂͂��悻100���l�ɂ̂ڂ�A�L�a����0.7?1.0���ƍl�����܂��B�@ |
|
| ��ʖ� |
�u�����h�� |
�̔���� |
�������� |
���l |
���i���^�j�R���_�a��
�@�I�����U�s�� |
�W�v���L�T*
Zyprexa |
�C�[���C�����[ |
508���~
�i2011/12�j |
2012�N ���E���� 1,701�S��$
1996/1 �č��Ŕ����B2001/4 ���{�Ŕ��� |
���^�R���_�a��
�@�t�}���_�N�G�`�A�s�� |
�Z���N�G��
Seroquel
* |
�A�X�g���[�l�J/�A�X�e���X���� |
264���~
�i2011/3�j |
2012�N ���E���� 2,803�S��$
2004/6 ���{�Ŕ��� |
���^�R���_�a��
�@���X�y���h��
|
���X�o�_�[�� |
J&J/�����Z���t�@�[�} |
295���~
�i2008�N�j |
2010�N ���E���� 1,500�S��$
1996/6 ���{�Ŕ��� |
���^�R���_�a��
�@�A���s�v���]�[�� |
�G�r���t�@�C |
��ː��� |
�@230���~
�i2011/3�j |
2010�N ���E���� 2,565�S��$
2002/11 �č��ŏ��F�B2006/06 ���{�Ŕ��� |
���^�R���_�a��
�@�W�v���V�h��
�i�]���̃Z���g�j��5-HT2�`����уh�p�~��D2��e�̂�I��I�ɎՒf�j |
ME2112 |
Meiji Seika�t�@���}/
���N�I���A�n�� |
������ |
2012/02/08 ���{�����ɂ�����Տ���II�������J�n
2011/03/14 ���C�Z���X�_�����
�{�܂́A�t�@�C�U�[���J�����A76�̍��ƒn��Ŕ̔�����A2010�N�̑S���E�ł̔����10���h���ȏ� |
���^�R���_�a��
�@�y���X�s���� |
���[���� |
����{�Z�F���� |
�@25���~
�i2011/3�j |
2001�N����
���Y���̃Z���g�j���E�h�[�p�~���h�R�� |
���^�R���_�a��
�@�����V�h�� |
���c�[�_ |
����{�Z�F���� |
69���~
�i2012/3�j
�k�� |
2012/10/25 ���B�\���i���c��i�H�Ɓj
2012/06/16 �J�i�_���F
2010/10/29 ����F
2011/10/27 PEARL 3 �����̌p�����^�����̌���
����P3�i���{�E�؍��E��p�̋��������j |
| �u���i���Z���� |
���i�Z�� |
����{�Z�F����
�g�x��i������� |
98���~
�i2012/3�j |
2008/04/21���� |
������e�̕W�I�^�̔��^�R���_�a��
asenapine |
SAPHRIS |
Merck & Co., Inc.
Meiji Seika�t�@���} |
������ |
2013/04/16 ���C�Z���X�_�����
MSD�����������NJ��҂�ΏۂɗՏ���V�����������{�� |
����R������������
�@�N���U�s�� |
�N���U���� |
�m�o���e�B�X �t�@�[�} |
�| |
2009/07/28 ���{�ɂ����ď��F |
����R������������
�@�p���y���h���p���~�`���_�G�X�e�� |
�C�����F�K |
�����Z���t�@�[�} |
�| |
2012/09/25 ���������ˍ܁i����^�j�̓��{�ɂ����鐻���̔����F�\��
�Z���g�j���T�|�g�s2A��e�̝h�R��p�A�h�p�~���c2��e�̝h�R��p��L����
2010/08/25 �������F���� |
| �V�K���������ǎ��Ö� |
AM-831 |
Meiji Seika�t�@���}/
�A�J�f�B�A |
�| |
2012/07/20 �J�����~
2009/03/25 ���C�Z���X�_����� |
| �O���V���Ď�荞�ݑj�Q�� |
RG-1678 |
���V�� |
�| |
2010/12/06 ��U���Տ������ʼnA���Ǐ�̉��P���F�߂�ꂽ |
|
|
�@ |
|
|
|
�@���a�͒N���������肤��a�C�ł����A����̎Љ�I�v������w�I�v���ɂ���Ĝ늳�������܂�܂��B�܂��ꕔ�̂��a�͈�`���̎����ł���A�O���̗L���Ɋւ�炸���ǂ��܂��B
�@���J�Ȃɂ��ƁA�Q�O�O�W�N�̎��E�Җ�R���Q��l�̂����A���@�Ƃ��ꂽ�̂́A���a���ő��Ŗ�U�S�O�O�l�B���a�𒆐S�Ƃ���u�C����Q�v�̐��_�����̊��Ґ��͓��N�A��P�O�S���l�ŁA�P�X�X�X�N����̂X�N�ԂŖ�U�O���l�������Ă��܂��B
�@���E�ی��@�ցiWHO�j�̓��v�ɂ��ƁA�S���E�Ŗ�1��2,100���l�̐l�����a�ɜ늳���Ă���Ƃ����Ă��܂��B�܂��A�ŐV�̌����ɂ��A���a�́A�g�̏�Q�̂����Ȍ��������Ƃ��ď��10�ʈȓ��ł���Ƃ���Ă��܂��B2020�N�܂łɂ͎��a�ʈ�Õ��S�z�̑�2�ʂɂ܂ŕ��シ���WHO�ł͗\�����Ă��܂�(�����FWHO�A2001�N��)�B
�@���{�ɂ����鎡�Ö�̎s��K�͖͂�1,000���~�Ɛ��肳��Ă��܂� |
|
| ��ʖ� |
�u�����h�� |
�̔���� |
�������� |
���l |
SSRI
�@�G�X�V�^���v���� |
���N�T�v��/�V�v�����b�N�X |
�����h�x�b�N/�t�H���X�g/���R���_�b�` |
�| |
2002�N�ɉ��ĂŔ����B
2008�N ���E���� 3,845�S��$ |
| ���N�T�v��R��10mg |
���c����
�i�c�ӎO�H�����j |
12���~
�i2012/3�j |
2011/07/21 ��������
���ϰ��@�����ޯ��Ђ��瓱��
�c�ӎO�H����Ƌ����̔����� |
SSRI
�@�p���L�Z�`�� |
�p�L�V�� |
�O���N�\�E�X�~�X�N���C��
����{�Z�F���� |
590���~
�i2008�N�j |
2012/01/19 ����{�Z�F����ƃR�E�v�����[�V����
1990�N�ɏ��߂ăC�M���X�ŏ��F�B���E40�����ȏ�ŏ��F
2000�N11���ɍ����Ŕ��� |
SSRI
�@�t���{�L�T�~���}���C���_�� |
�f�v�����[�� |
Meiji Seika�t�@���} |
92���~
�i2009/3�j |
2011/06/21 �A�X�e���X����A�{�b�g �W���p���֔̔��ڊ�
���{�ōŏ��ɔ������ꂽSSRI |
| ���{�b�N�X |
�A�X�e���X���� |
82���~
�i2011/3�j |
SSRI
�@���_�Z���g������ |
�]���t�g
�W�F�C�]���t�g |
�t�@�C�U�[ |
�| |
1991�N�ɕĂŏ��F
���{�@2006�N7�����F
2010/07/07 �p�j�b�N��Q�̓�d�ӌ���r��������
2010�N ���E���� 532�S��$ |
SSRI
�@�t���I�L�Z�`�� |
�v���U�b�N |
�C�[���C�����[ |
�| |
1988�N�ɕĂŏ��F
���{�ł͖����F |
SNRI
�@�y�����t�@�L�V�� |
�G�t�F�N�T�[XR |
�t�@�C�U�[/�A���~���� |
�| |
2010�N ���E���� 1,718�S��$ |
SNRI
�@�f�����L�Z�`�����_�� |
�T�C���o���^ |
�C�[���C�����[/�x�[�����K�[�C���Q���n�C��
�����[/����`����
|
34���~
�i2010/12�j
27���~
�i2011/3�j |
2004�N�č��Ŕ����A95�J���ŏ��F
2010�N ���E���� 3,480�S��$
2010�N1���@���{�ŏ��F |
SNRI
�@�~���i�V�v���� |
�g���h�~�� |
�������t�@�[�}/�����Z���t�@�[�} |
50���~
�i2010/3�j |
���{�ōŏ��ɔF���ꂽSNRI
2000�N9���ɍ����Ŕ��� |
SNRI
�@�f�X�x�����t�@�L�V�� |
�@ |
�t�@�C�U�[ |
�| |
�@ |
�R���_�a��
�@�V�K�h�p�~��D2��e�̃p�[�V�����E�A�S�j�X�g |
ABILIFY |
��ː��� |
�| |
2012/02/06�@���B�ɂĐN���̑o�� I �^��Q*1�ɂ����钆���x����d�x���N�Ǐ�̉��P�ɑ���K���lj��̎擾 |
�R���_�a��
�@�I�����U�s�� |
�W�v���L�T*
Zyprexa |
�C�[���C�����[ |
�| |
2012/02/22�@�������F�i�o�ɐ���Q�ɂ����邤�Ǐ�̉��P�j
���^�R���_�a��ŁA1996�N�ɕč��œ��������ǎ��Ö�Ƃ��Ĕ��� |
NaSSA
�@�~���^�U�s�� |
��������/���t���b�N�X |
Merck & Co., Inc./Meiji Seika�t�@���} |
�| |
1994�N �I�����_�Ŕ���
2009�N9���@���{�Ŕ���
2010�N ���E���� 223�S��$ |
���̎O�n�R����
�@���_�N���~�v���~���� |
�A���L�T�� |
�t�@�C�U�[ |
�| |
�@ |
�`�G�m�W�A�[�s���n�R�s����
�@�G�`�]���� |
�f�p�X |
�c�ӎO�H���� |
114���~
�i2011/3�j |
1983�N9�� ���{�ɂď��F
�����̌㔭���i������ |
�Z���g�j���쓮���R�s����
�@�G�`�]���� |
�Z�f�B�[�� |
����{�Z�F���� |
�| |
�@ |
�x���]�W�A�[�s���n�R�s����
�@���t���[�v�_�G�`�� |
���C���b�N�X |
Seika�t�@���} |
�| |
1989�N9�� ���{�ɂĔ���
�����̌㔭���i������ |
�x���]�W�A�[�s���n�R�s����
�@�����[�p�� |
���C�p�b�N�X |
�t�@�C�U�[ |
�| |
�@ |
���^�R���_�a��.
�@�����V�h�����_�� |
LATUDA |
����{�Z�F���� |
�| |
2012/06/29�@�č��ɂ�����o�ɇT�^��Q���ɑ���K���lj����F�擾�`���E�� |
���d��p���J�j�Y���^�R����
�{���`�I�L�Z�`���L�����f�_�� |
Brintellix
Lu AA21004 |
H. Lundbeck A/S
���c��i�H�� |
�| |
2014/01/21�@�����
2011/05/14�@�����o�R�����J�n
���B �o�|�V
Lundbeck�ЋN�� |
| ���m�A�~�����ߖ� |
Lu AA24530 |
H. Lundbeck A/S
���c��i�H�� |
�| |
���݁A�̔�����Ă���R���܂Ƃ͈قȂ��p�@����L����
2010/03/03�@�o�|�V�̊J�n������
2007/10/24�@���B �o�|�U
���{ �o�|�T
Lundbeck���N�� |
�V�K�h�p�~��D2��e�̃p�[�V�����E�A�S�j�X�g
�u���N�X�s�v���]�[�� |
OPC-34712 |
��ː���
. Lundbeck A/S |
�| |
2014/01/24�@P3�������ʂ����B���_�Ȋw��c�iEPA 2014�j�Ŕ��\�F
2011/05/16�@�傤�a�ɑ���Տ���II�������ŗL�p�����m�F |
|
|
��SSRI�F�I��I�Z���g�j���Ď�荞�ݑj�Q��B���݁A�R���܂̂V�O���ȏ���߂�
��SNRI�F�Z���g�j���E�m���A�h���i�����Ď�荞�ݑj�Q��B�r�r�q�h�̎�����̍R����
��NaSSA�F�m���A�h���i�����쓮���E���ٓI�Z���g�j���쓮���R����BSSRI��SNRI�Ƃ͈قȂ��p�@�������� |
|
�@ |
|
|
|
�@�s���ǂ͑S�l���̖�P�����늳���Ă���Ƃ���鐇����Q�ŁA�Q��������(������Q)�A�����Ă��r���ʼn��x���ڂ��o�߁A���̌�Ȃ��Ȃ��Q�t���Ȃ��i���r�o���j�ȂǁA�����Ɋւ�1�ȏ�̖�������A�����̐����@�\�Ɏx������������Ƃ�����܂��B�s���NJ��҂͒j�����������ɑ����A�ǂ̔N��ł����ǂ���\��������܂����A����ƂƂ��ɜ늳�����オ���Ă��܂��B
�@���ݓ��{�ł͖�2,400���l�̕��X��������Q�ŔY��ł���Ɛ��肳��Ă���A����܂��܂��������邱�Ƃ��\�z����Ă��܂��B���Ö�̎s��K�͖͂�V�U�O���~�Ɛ��肳��Ă��܂��B |
|
| ��ʖ� |
�u�����h�� |
�̔���� |
�������� |
���l |
�f�`�a�`�|�`��e�̍쓮��i�x���]�W�A�[�s���n��܁j
�@���Z���Ԍ^
�@�@�g���A�]���� |
�n���V�I�� |
�t�@�C�U�[ |
�| |
�㔭�i�F
�@�~���U�C���i����H�j
�@�n�����b�N�i�x�m��i�j
�@�p�����I���i��m��i�j
�@�A�T�V�I���i����������j
�@�J�����g���i������j |
�@�Z���Ԍ^
�@�@�u���`�]���� |
�����h���~�� |
�x�[�����K�[�C���Q���n�C�� |
139���~
�i2008/12�j |
�@ |
| �@�@���_�����}�U�z�� |
���X�~�[ |
����`���� |
�| |
1989�N�@�������F |
| �@�@�������^�[�p�� |
�G�o�~�[�� |
�o�C�G����i |
�| |
1990�N�@�������F |
| �@�@�������^�[�p�� |
�������b�g |
�t�@�C�U�[ |
�| |
�@ |
�@���Ԍ^
�@�@�t���j�g���[�p�� |
���q�v�m�[�� |
���O���� |
�| |
1970�N��O���Ƀ��V�����J�� |
| �@�@�t���j�g���[�p�� |
�T�C���[�X |
�G�[�U�C |
�| |
�@ |
| �@�@�G�X�^�]���� |
���[���W�� |
���c��i�H�� |
�| |
�@ |
| �@�@�j�g���[�p�� |
�x���U���� |
����`���� |
�| |
�@ |
| �@�@�N�A�[�p�� |
�h���[�� |
�v������ |
�| |
1999�N�@�������F |
�@�����Ԍ^
�@�@�n���L�T�]���� |
�\������ |
���O�� |
�| |
1981�N�@�������F |
| �@�@���_�t�����[�p���J�v�Z�� |
�_�����[�g |
���a��i |
�| |
�@ |
| �@�@�t�����[�p�� |
�C���X�~�� |
�L���[�������� |
�| |
�@ |
�i��x���]�W�A�[�s���n��܁j
�@���Z���Ԍ^
�@�@�]�s�N���� |
�A���o�� |
�T�m�t�B�E�A�x���e�B�X |
51���~
�i2009/12�j |
1989�N�@�������F
�����[�k�E�v�[�������[���[�N�� |
| �@�@��Ύ_�]���s�f�� |
�}�C�X���[ |
�T�m�t�B�E�A�x���e�B�X/
�A�X�e���X���� |
327���~
�i2011/3�j |
���E���� 819�S��EUR |
| �@�@�]���s�f����Ύ_�� |
�]���s�f����Ύ_���� |
����{�Z�F���� |
�| |
2012/02/20 �������F�i�W�F�l���b�N���i�j |
GABA-A��e�̍쓮��i��x���]�W�A�[�s���n����j
�@�G�X�]�s�N���� |
���l�X�^ |
�Z�v���R�[��/����{�Z�F���� |
�| |
2004�N12���@����F�i�Z�v���R�[���j
����� 421���~�i2012/03�j
�č��ōł�����Ă��鐇����Ŗ�40���̃V�F�A���m��
�������ԁF2014�N2���܂� |
| �G�[�U�C |
�| |
2012/01/18 �������F
�Z�v���R�[���i����{�Z�F����j�N�� |
�����g�j����e�̍쓮��
�@�������e�I�� |
���[���� |
���c��i�H�� |
25���~
�i2012/3�j |
2011/10/07�@���B�J�����~
2005�N7���@����F
2010/04/16�@�������F |
| �f���A���I���L�V����e�̝h�R���@ |
MK-4305
�X�{���L�T���g |
MSD |
�| |
2013/07/03 FDA���R�������ʒm�����
2012/12/04 �����\�� |
|
|
���P �x���]�W�A�[�s���n��܁G ���ÁE�Ö���p�̂ق��C����p�Ƃ��čR�s����p�C�^����Q��p�C�ؒo�ɍ�p���������܂��B
���Q ��x���]�W�A�[�s���n��܁F ����p���ጸ����Ă���̂ŁC�}���Ɏg�p����Ă��Ă��܂��B
���R �����g�j���쓮�܁F �]���̕s���ǎ��Í܂Ƃ͍�p�@�����قȂ�܂��B�K�����̔F�߂��Ȃ��s���ǎ��Ö�Ƃ��Ċ��҂���Ă��܂��B |
|
�@ |
| �i�Ꮎ���j |
|
|
|
| ��ʖ� |
�u�����h�� |
�̔���� |
�������� |
���l |
�Γ���E���ሳ�ǎ��Í�
�@�^�t���v���X�g |
�^�v���X�~�j�_��t 0.0015�� |
�Q�V���� |
�| |
2013/01/18 �������F |
�Γ���E���ሳ�ǎ��Í�
�@�u�����j�W����Ύ_�� |
�A�C�t�@�K���_��t 0.1% |
������� |
�@ |
2012/05/11 �������� |
�Γ���E���ሳ�ǎ��Í�
�@�u�����j�W����Ύ_�� |
�A�C�t�@�K���_��t 0.1% |
�L���[�������� |
�@ |
2012/04/20 ��������
�č��A���K���Ђ�蓱��
�������ɓ��o |
�Γ���E���ሳ�ǎ��Í�
�@�g���{�v���X�g�E�`�����[���}���C���_�� |
�f���I�g���o�z���_��t |
���{�A���R�� |
�@�@ |
2010/04/16 �������F |
�Γ���E���ሳ�ǎ��Í�
�@�h���]���~�h���_���^�`�����[���}���C���_�� |
�R�\�v�g�z���_��t |
MSD
�Q�V���� |
�@ |
2010/04/16 �������F |
�Γ���E���ሳ�ǎ��Í�
�@���^�m�v���X�g�E�`�����[���}���C���_�� |
�U���J���z���_��t |
�t�@�C�U�[ |
�@ |
2010/01/20 �������F
���{���̗Γ��Ꭱ�Ôz����
2012�N ���E����806�S���� |
�Γ���E���ሳ�ǎ��Í�
�@�^�t���v���X�g |
�^�v���X�_��t 0.0015�� |
�Q�V���� |
�@ |
2008/10/17 �������F |
| �Γ���E���ሳ�ǎ��Í� |
���^�m�v���X�g�_��t |
�@ |
�@ |
�v���X�^�O�����W���U���̂ł���v���X�g�n�Γ���E���ሳ�ǎ��Ö� |
| �Γ���E���ሳ�ǎ��Í� |
���X�L����R�_��t |
�@ |
�@ |
��ӌ^�v���X�^�O�����W���U���̂ł���v���X�g�����g�������E���̗Γ���E���ሳ�ǎ��Ö� |
�Γ���E���ሳ�ǎ��Í�
�@ |
�J���R�[�h�FK-115 |
���a |
�@ |
2011/05/09 P2���ʔ��\
Rho �L�i�[�[�j�Q��p��L���� |
|
|
�@ |
|
|
|
| ��ʖ� |
�u�����h�� |
�̔���� |
�������� |
���l |
���o�^������ϐ����Â̂��߂���ȗpVEGF�j�Q��
�@�A�t���x���Z�v�g�i��`�q�g�����j |
�A�C���[�AR�Ɏq�̓����ˉt40mg/mL |
�o�C�G����i
�Q�V���� |
�| |
2012/11/27 �������� |
�@���j�r�Y�}�u�i��`�q�g�����j |
���Z���e�B�X�Ɏq�̓����ˉt2.3�~���O����/0.23�~���O����
Lucentis |
�m�o���e�B�X�t�@�[�} |
�@ |
2012�N ���E���� 2,398�S��$
2009/01/21 �������F |
������ϐ��ǎ��Í�
�@�y�K�v�^�j�u�i�g���E�� |
�}�N�W�F���Ɏq�̓����˗p�L�b�g0.3mg |
�t�@�C�U�[ |
�@ |
2008/10/14 ��������
���{���̃A�v�^�}�[���i |
|












